ธาตุกัมมันตรังสี

ความหมายของธาตุกัมมันตรังสี
ธาตุกัมมันตรังสี หมายถึงธาตุที่แผ่รังสีได้ เนื่องจากนิวเคลียสของอะตอมไม่เสถียร เป็นธาตุที่มีเลขอะตอมสูงกว่า 82
กัมมันตภาพรังสี หมายถึงปรากฏการณ์ที่ธาตุแผ่รังสีได้เองอย่างต่อเนื่อง รังสีที่ได้จากการสลายตัว มี 3 ชนิด คือ รังสีแอลฟา รังสีบีตา และรังสีแกมมา
ในนิวเคลียสของธาตุประกอบด้วยโปรตอนซึ่ง มีประจุบวกและนิวตรอนซึ่งเป็นกลางทางไฟฟ้า สัดส่วนของจำนวนโปรตอนต่อจำนวนนิวตรอนไม่เหมาะสมจนทำให้ธาตุนั้นไม่เสถียร ธาตุนั้นจึงปล่อยรังสีออกมาเพื่อปรับตัวเองให้เสถียร ซึ่งเป็นกระบวนการที่เกิดขึ้นเองตามธรรมชาติ เช่น
จะเห็นได้ว่า การแผ่รังสีจะทำให้เกิดธาตุใหม่ได้ หรืออาจเป็นธาตุเดิมแต่จำนวนโปรตอนหรือนิวตรอนอาจไม่เท่ากับธาตุเดิม และธาตุกัมมันตรังสีแต่ละธาตุ มีระยะเวลาในการสลายตัวแตกต่างกันและแผ่รังสีได้แตกต่างกัน เรียกว่า ครึ่งชีวิตของธาตุ
กัมมันตภาพรังสี (radioactivity) เกิดจากการเสื่อมสลายโดยตัวเองของนิวเคลียสของอะตอมที่ไม่เสถียร เป็นผลให้ได้อนุภาคอัลฟา อนุภาคเบต้า และรังสีแกมมาซึ่งเป็นคลื่นแม่เหล็กไฟฟ้าที่มีช่วงคลื่นสั้นมากและมีพลังงาน สูง ทั้งหมดนี้พุ่งออกมาด้วยความเร็วสูงมาก ในบางกรณีอาจมีพลังงานความร้อนและพลังงานแสงเกิดตามมาด้วย เช่น การเสื่อมสลายของนิวเคลียสของธาตุเรเดียมไปเป็นธาตุเรดอน
คำว่ากัมมันตภาพรังสีนี้ มีหลายคนใช้ผิด โดยสับสนกับคำว่า กัมมันตรังสี ซึ่งจะขออธิบายดังนี้
กัมมันตภาพรังสี (Radioactivity) เป็นคำนาม หมายถึง สภาพการแผ่รังสีของธาตุหนึ่ง ๆ ที่ไม่เสถียร เช่น O-18 เป็นต้น
กัมมันตรังสี (Radioactive) เป็นคำคุณศัพท์ ส่วนใหญ่ใช้ขยายคำว่าธาตุ คือ ธาตุกัมมันตรังสี หมายถึง ตัวธาตุที่ปล่อยรังสี (อนุภาคอัลฟา อนุภาคเบต้า และรังสีแกมมา) ออกมา
กัมมันตภาพรังสี...คืออะไร?
กัมมันตภาพรังสี (Radioactivity) เป็นคุณสมบัติของธาตุและไอโซโทปบางส่วน ที่สามารถเปลี่ยนแปลงตัวเองเป็นธาตุหรือไอโซโทปอื่น ซึ่งการเปลี่ยนแปลงนี้จะมีการปลดปล่อยหรือส่งรังสีออกมาด้วย ปรากฏการณ์นี้ได้พบครั้งแรกโดย เบคเคอเรล เมื่อปี พ.ศ. 2439 ต่อ มาได้มีการพิสูจน์ทราบว่า รังสีที่แผ่ออกมาในขบวนการสลายตัวของธาตุหรือไอโซโทปนั้นประกอบด้วย รังสีแอลฟา, รังสีเบต้า และรังสีแกมมา
รังสีแอลฟา
รังสีที่ประกอบด้วยอนุภาคแอลฟาซึ่งเป็นอนุภาคที่มีมวล 4 amu มีประจุ +2 อนุภาคชนิดนี้จะถูกกั้นไว้ด้วยแผ่นกระดาษหรือเพียงแค่ผิวหนังชั้นนอกของคนเราเท่านั้น
การสลายตัวให้รังสีแอลฟา
90Th 232----->88Ra 228 + 2a 4
รังสีเบต้า
รังสี ที่ประกอบด้วยอนุภาคอิเลคตรอนหรือโพสิตรอน รังสีนี้มีคุณสมบัติทะลุทะลวงตัวกลางได้ดีกว่ารังสีแอลฟา สามารถทะลุผ่านน้ำที่ลึกประมาณ 1 นิ้วหรือประมาณความหนาของผิวเนื้อที่ฝ่ามือได้ รังสีเบต้าจะถูกกั้นได้โดยใช้แผ่นอะลูมิเนียมชนิดบาง
การสลายตัวให้รังสีบีตา
79Au 198----->80Hg 198 + -1b 0
7N 13----->6C 13 + +1b 0
รังสีแกมมา
รังสี ที่เป็นคลื่นแม่เหล็กไฟฟ้าพลังงานสูง มีคุณสมบัติเช่นเดียวกันกับรังสีเอกซ์ที่สามารถทะลุผ่านร่างกายได้ การกำบังรังสีแกมมาต้องใช้วัสดุที่มีความหนาแน่นสูงเช่น ตะกั่วหรือยูเรเนียม เป็นต้น
การสลายตัวให้รังสีแกมมา
27Co 60----->-1b 0 + 28Ni 60----->28Ni60 + g
ประวัติการค้นพบกัมมันตภาพรังสี
ผู้ค้นพบกัมมันตภาพรังสี คือ เฮนรี เบคเคอเรล เป็นชาวฝรั่งเศส อ็องตวน อ็องรี เบ็กแรล (ฝรั่งเศส: Antoine Henri Becquerel, /bekʀɛl/; 15 ธันวาคม พ.ศ. 2395 – 25 สิงหาคม พ.ศ. 2451) นักฟิสิกส์ชาวฝรั่งเศส เกิดในตระกูลที่มีนักวิทยาศาสตร์ถึง 4 รุ่น ตั้งแต่รุ่นปู่จนกระทั่งรุ่นลูก เขาได้รับรางวัลโนเบลสาขาฟิสิกส์ในปี พ.ศ. 2446 ร่วมกับปีแยร์ กูรี และมารี กูรี หลังจากที่เขาถึงแก่กรรม ชื่อสกุลของเขาได้กลายเป็นหน่วยวัดกัมมันตภาพ ในระบบหน่วยเอสไอ คือ เบ็กแรล เขียนด้วยสัญลักษณ์ Bq
อ็องรี เบ็กแรล นักฟิสิกส์ชาวฝรั่งเศส
ชีวิตส่วนตัว
อ็องรี เบ็กแรล เกิดที่กรุงปารีส โดยเป็นบุตรของอาแล็กซ็องดร์-แอดมง เบ็กแรล (Alexandre-Edmond Becquerel) ซึ่งเป็นนักฟิสิกส์ที่ศึกษาเกี่ยวกับทัศนศาสตร์ ไฟฟ้า และแม่เหล็ก อ็องรีได้เข้าเรียนในโรงเรียน เอกอลปอลีแต็กนิก (École Polytechnique) ซึ่งเป็นโรงเรียนช่างฝีมือทหารของฝรั่งเศส และต่อมาก็เข้าเรียนใน เอกอลเดปงเซโชเซ (École des Ponts et Chaussées) ซึ่งเป็นโรงเรียนที่สอนวิชาวิศวกรรมศาสตร์ที่เก่าแก่แห่งหนึ่ง ในด้านชีวิตครอบครัว อ็องรีสมรสกับหลุยส์ เดซีเร ลอรีเยอ (Louise Désirée Lorieux) มีบุตร 1 คน คือ ฌ็อง เบ็กแรล (Jean Becquerel) ซึ่งก็ได้เป็นนักฟิสิกส์เช่นเดียวกับอ็องรี ต่อมา ในปี พ.ศ. 2451 อ็องรีได้รับเลือกให้เป็นเลขาธิการวิทยาลัยวิทยาศาสตร์แห่งฝรั่งเศส (Académie des Sciences) และถึงแก่กรรมที่เลอครัวซี (Le Croisic) ในแคว้นเบรอตาญ ในปีเดียวกันกับที่ได้รับเลือก
[แก้] ชีวิตการงาน และงานวิจัยที่สำคัญ
ภาพหมอกจากแผ่นฟิล์มที่อ็องรี เบ็กแรลได้ทดลองนำกัมมันตภาพรังสีมาวางบนแผ่นฟิล์มที่ปกปิดอย่างดี แต่ก็ไม่อาจต้านทานการทะลุทะลวงได้
ในปี พ.ศ. 2435 อ็องรีได้เป็นคนที่สามในตระกูลเบ็กแรล ที่ได้เป็นภัณฑารักษ์ส่วนฟิสิกส์ที่พิพิธภัณฑ์ประวัติศาสตร์ธรรมชาติแห่ง ชาติฝรั่งเศส (Muséum National d'Histoire Naturelle) อีกสองปีให้หลัง เขาได้รับตำแหน่งหัวหน้านายช่างประจำกรมการสะพานและทางหลวง
นับจากที่ได้รับตำแหน่งหัวหน้านายช่าง 2 ปี อ็องรีได้ศึกษาการเรืองแสงอย่างช้า (phosphorescence) ในเกลือยูเรเนียม จนเขาได้พบกัมมันตรังสีเข้า โดยบังเอิญ โดยเขาได้วางโพแทสเซียมยูเรนิลซัลเฟต ซึ่งตกทอดมาจากพ่อของเขา ไว้บนฟิล์มถ่ายรูปและวัสดุดำ จากนั้นนำไปตั้งไว้กลางแดด โดยเขาได้อธิบาย ณ ที่ประชุมวิทยาลัยวิทยาศาสตร์แห่งฝรั่งเศส มีใจความดังนี้
เมื่อหุ้มฟิล์มถ่ายรูปลูมีแยร์ด้วยกระดาษดำหนา ๆ ซึ่งมีสารพวกโบรไมด์คั่น อยู่ ฟิล์มนั้นจะไม่มีลายหมอก แม้ตั้งไว้กลางแดดจ้า เมื่อวางสารนั้น (โพแทสเซียมยูเรนิลซัลเฟต) บนกระดาษซึ่งทับห่อนั้น จากนั้นนำไปวางไว้กลางแดด แล้วเอาฟิล์มนั้นมาล้าง จะพบว่ามีลายหมอกเป็นสีดำบนภาพเนกะทีฟ (ภาพที่ยังไม่ได้อัด) เมื่อใดที่เอาวัตถุอื่นใดปกปิดสารนั้น แล้วทดลอง ก็ปรากฏรูปวัตถุนั้น ๆ บนฟิล์ม...ดังนั้นจึงสรุปว่า สารนั้นมีกัมมันตรังสีจริง รังสีนั้นผ่านทะลุกระดาษหนา ๆ ได้ และรีดิวซ์เงินได้ |
การค้นพบกัมมันตภาพรังสีของเบคเคอเรล เป็นการค้นพบขณะที่เขากำลังศึกษาแสงแดดเป็นตัวการที่ทำให้ธาตุยูเรเนียมปลด ปล่อยรังสีเอ็กซ์ บังเอิญช่วงการทดลองไม่มีแสงแดดเป็นเวลา 2- 3 วัน ชุดทดลองของเขาซึ่งเก็บไว้ในลิ้นชักไม่ถูกแสงแดด แต่เมื่อเขานำฟิล์มที่มีกระดาษห่อสารยูเรเนียมไปล้าง ปรากฏว่าที่ฟิล์มมีการเปลี่ยนแปลงที่เข้มกว่าช่วงถูกแสงแดดเบคเคอเรล จึงคิดว่าน่าจะมีรังสีบางอย่างถูกปลดปล่อยออกมาจากธาตุนั้นตลอดเวลา
เมื่อเขาศึกษาต่อ พบว่า มีธาตุบางชนิดจะปลดปล่อยรังสีออกมาตลอดเวลา เรียกธาตุนั้นว่าธาตุกัมมันตรังสี และรังสีที่ธาตุนั้นปลดปล่อยออกมาเรียกว่ากัมมันตภาพรังสี ซึ่งมี 3 ชนิด คือรังสีแอลฟา รังสีเบตา และรังสีแกมมา
นอกจากเบคเคอเรลแล้ว นักวิทยาศาสตร์ที่ศึกษาเกี่ยวกับธาตุกัมมันตรังสี และกัมมันตภาพรังสีจนได้รับรางวัลโนเบล คือ มารี คูรี.
- มารี คูรี.
มารี กูรี (โปแลนด์: Marya Skłodowska; อังกฤษ: Marie Curie) (7 พฤศจิกายน 2410 - 4 กรกฎาคม 2477) นักเคมีผู้ค้นพบรังสีเรเดียม ที่ใช้ยับยั้งการขยายตัวของมะเร็ง ซึ่งเป็นโรคร้ายที่ไม่สามารถรักษาให้หายขาดได้ แต่มีอัตราการตายของของคนไข้เป็นอันดับหนึ่งมาทุกยุคสมัย ด้วยผลงานที่มีความสำคัญต่อมนุษยชาติเหล่านี้ ทำให้มารี กูรีได้รับรางวัลโนเบลถึง 2 ครั้งด้วยกัน
มารี เป็นชาวโปแลนด์ เกิดเมื่อวันที่ 7 พฤศจิกายน พ.ศ. 2410 ที่เมืองวอร์ซอ เขตวิสทูลา จักรวรรดิรัสเซีย ซึ่งปัจจุบันเป็นประเทศโปแลนด์[1]ครูสอนวิทยาศาสตร์ และมักพาเธอมาที่ห้องทดลองเสมอ จึงทำให้เธอสนใจวิชาด้านวิทยาศาสตร์ตั้งแต่เด็ก แม้จะมีเหตุการณ์ทางการเมืองเมื่อรัสเซียมาปกครองโปแลนด์ และบังคับให้ใช้ภาษารัสเซียเป็นภาษาทางการก็ตาม บิดาเป็น
หลังจบการศึกษาระดับต้นแล้ว เธอกับพี่สาวก็ทำงานด้วยการเป็นครูอนุบาล สอนหนังสือให้กับเด็กๆ แถวๆ นั้น โดยทั้งสองมุ่งหวังอยากไปเรียนต่อที่ฝรั่งเศส แต่เงินไม่พอกับค่าใช้จ่าย เธอจึงให้พี่สาวคือ บรอนยา ไปเรียนต่อด้านแพทย์ศาสตร์ก่อน พอจบแล้วค่อยส่งเสียเธอเรียนต่อด้านวิทยาศาสตร์ต่อไป จนพี่สาวจบมาเธอก็ได้ไปเรียนต่อที่ มหาวิทยาลัยปารีส สมใจแต่ด้วยเงินอันน้อยนิดจากพี่สาว ไม่พอต่อค่าใช้จ่ายเธอจึงดิ้นรนหางานทำ จนได้เป็นผู้ช่วยในห้องปฏิบัติการทางเคมี ของ ปิแอร์ กูรี จนทั้งสองแต่งงานมีลูกด้วยกัน แต่ ปิแอร์ เสียชีวิตก่อนเพราะอุบัติเหตุรถม้าชน ระหว่างที่เรียนไปทำงานไป เธอก็มุ่งมั่นศึกษาทดลองไปเรื่อยๆ จนมาพบรังสีแร่ธาตุเรเดียม โดยได้มาจากแร่พิทช์เบลนที่เป็นออกไซต์ชนิดหนึ่งสามารถแผ่รังสีได้ จากการเพียรพยายามทดลองมาหลายปีในการสกัดแร่ชนิดต่างๆ จนมาพบรังสีดังกล่าวทำให้เธอได้รับปริญญาเอก ในการค้นพบแร่ธาตุเรเดียม
จนในปี พ.ศ. 2445 (ค.ศ. 1902) เธอก็สามารถสกัดแร่เรเดียมให้บริสุทธิ์ได้ เรียกว่า เรเดียมคลอไรด์ ที่สามารถแผ่รังสีได้มากกว่ายูเรเนียมถึง 2,000,000 เท่า มีคุณสมบัติคือ ให้แสงสว่าง และความร้อนได้ และเมื่อแร่นี้แผ่รังสีไปถูกวัตถุอื่น วัตถุนั้นจะเปลี่ยนสภาพเป็นธาตุกัมมันตรังสี และสามารถแผ่รังสีได้เช่นเดียวกันกับแร่เรเดียม จนทำให้เธอได้รับรางวัลโนเบลต่อมา
มารี กูรี
การศึกษาค้นคว้าเกี่ยวกับแร่เรเดียมอย่างหนัก และต่อเนื่องกว่า 4 ปี ทำให้เธอได้รับรางวัลโนเบลอีกครั้ง แม้สามีจะเสียชีวิตก็ตาม ด้วยกำลังใจอันล้นเปี่ยม เมื่อเกิดภาวะสงครามโลกครั้งที่ 1 ซึ่งผู้คนส่วนมากล้มตายและถูกเกณฑ์ไปเป็นทหาร เธอจึงอาสาสมัครเป็นอาสากาชาดเพื่อช่วยทหารที่บาดเจ็บ ในการเอกซเรย์เคลื่อนที่ตระเวนรักษาตามหน่วยต่างๆ จนสงครามสงบเธอก็กลับมาทำงาน แต่ก็ต้องล้มป่วยเพราะผลมาจากการทำงานหนัก และโดนรังสีเรเดียม ทำให้ไขกระดูกถูกทำลายและเสียชีวิตในเวลาต่อมา
รางวัลที่ได้รับ
ประกาศนียบัตรรางวัลโนเบลของมารี กูรี
- รางวัลโนเบลสาขาฟิสิกส์ ค.ศ. 1903 จากผลงานการพบธาตุเรเดียม[3]
- Davy Medal ค.ศ. 1903
- Matteucci Medal ค.ศ. 1904
- รางวัลโนเบลสาขาเคมี ค.ศ. 1911 จากผลงานการค้นคว้าหาประโยชน์จากธาตุเรเดียม
วิลเฮล์ม คอนราด เรินต์เกน (Wilhelm Conrad Röntgen - 27 มีนาคม พ.ศ. 2388 — 10 กุมภาพันธ์ พ.ศ. 2466) นักฟิสิกส์ชาวเยอรมัน ประจำมหาวิทยาลัยเวิร์ซแบร์ก ผู้ค้นพบและสร้าง รังสีแม่เหล็กไฟฟ้า ที่มี ช่วงคลื่น ขนาดที่รู้จักในปัจจุบันว่า รังสีเอกซ์ (x-rays) หรือ รังสีเรนต์เกน เมื่อวันที่ 8 พฤศจิกายน พ.ศ. 2438ความสำเร็จที่ทำให้เรินต์เกนได้รับรางวัลโนเบลรางวัลแรก เมื่อ พ.ศ. 2444

Röntgen” มักสะกดเป็นภาษาอังกฤษโดยทั่วไปว่า “Roentgen” ดังนั้น ในเอกสารวิชาการและการแพทย์เกือบทั้งหมดจึงใช้คำสะกดว่า “Roentgen”
ชีวิตในวัยเยาว์และการศึกษา
เรินต์ เกน เกิดที่เมืองเลนเนพ ปัจจุบันอยู่ในแคว้นเร็มส์ไชด์ ประเทศเยอรมนี บิดามารดาเป็นช่างตัดเย็บเส้อผ้า ต่อมาได้ย้ายครอบครัวไปตั้งรกรากที่เอเปลดูร์น ประเทศเนเธอร์แลนด์ เมื่อเรินต์เกนอายุได้ 3 ขวบ เรินต์เกนได้รับการศึกษาขั้นต้นที่สถาบันแห่งมาร์ตินุส เฮอร์มัน แวน เดอร์ดูร์น ต่อมาได้เข้าเรียนในสถาบันเทคนิคอูเทรชต์ ที่ซึ่งเขาถูกไล่ออกจากสถาบันเนื่องจากถูกกล่าวหาว่าเขียนภาพล้ออาจารย์คน หนึ่ง ซึ่งเรินต์เกนไม่เคยยอมรับว่าเป็นผู้เขียน
ใน พ.ศ. 2408 เรินต์เกนพยายามสมัครเข้าเรียนที่มหาวิทยาลัยอูเทรชต์โดยไม่มีเอกสารหลักฐาน ที่จำเป็นสำหรับนักศึกษาปกติแต่ไม่ได้รับการรับเข้าเรียน ต่อมาเรินต์เกนทราบว่าที่สถาบันโปลีเทคนิคในซุริก (ปัจจุบันคือ ETH Zurich ที่ มีชื่อเสียง) รับนักศึกษากรณีนี้เข้าเรียนได้โดยการสอบ เขาจึงเริ่มการศึกษาระดับมหาวิทยาลัยสาขาวิศวกรรมเครื่องกล ในปี พ.ศ. 2412 เรินต์เกนจบการศึกษาระดับปริญญาเอกจากมหาวิทยาลัยซูริกแห่งนี้
การทำงาน
ในปี พ.ศ. 2410 เรินต์เกนเข้าทำงานเป็นอาจารย์ที่มหาวิทยาลัยสตราสบวร์ก และในปี พ.ศ. 2414 ได้เป็นศาสตราจารย์ในสถาบันเกษตรศาสตร์ที่ฮอเฮนไฮม์ เวิร์ทเตมเบิร์ก เรินต์เกนได้กลับไปเป็นศาสตราจารย์สาขาวิชาฟิสิกส์ที่มหาวิทยาลัยสตราสบวร์ กอีกคร้งหนึ่งเมื่อ พ.ศ. 2419 และในปี พ.ศ. 2422 เรินต์เกนได้รับการแต่งตั้งเป็นหัวหน้าภาควิชาฟิสิกส์ที่มหาวิทยาลัยไกส์เซน พ.ศ. 2431 ย้ายไปรับตำแหน่งหัวหน้าภาควิชาฟิสิกส์ที่มหาวิทยาลัยเวิร์ซเบิร์ก และอีกครั้งที่มหาวิทยาลัยมิวนิกในปี พ.ศ. 2443 โดยคำขอของรัฐบาลบาวาเรีย
เรินต์เกนมีครอบครัวอยู่ในประเทศสหรัฐฯ ที่รัฐโอไฮโอ ครั้งหนึ่งเขาเคยคิดที่จะย้ายไปตั้งรกรากที่นั่น เรินต์เกนได้ยอมรับการแต่งตั้งที่มหาวิทยาลัยโคลัมเบีย ในนิวยอร์ก และได้ซื้อตั๋วเรือไว้แล้ว แต่การระเบิดของสงครามโลกครั้งที่ 1 ทำให้แผนการนี้เปลี่ยนไป เรินต์เกนตกลงอยู่ในมิวนิกต่อไปและได้ทำงานที่นี้ไปตลอดชีวิต เรินต์เกนถึงแก่กรรมเมื่อปี พ.ศ. 2456 จากโรคมะเร็งเยื่อบุช่องท้อง มีการพูดกันว่าเรินต์เกนเสียชีวิตจากการได้รับรังสีเอกซ์เรย์ แต่ส่วนใหญ่ไม่เชื่อว่าการเกิดโรคมะเร็งนี้เป็นผลมาจากการรับรังสีเอกซ์เรย์ ทั้งนี้เนื่องจากการค้นคว้าวิจัยในส่วนที่เรินต์เกนต้องเกี่ยวข้องกับรังสี โดยตรงและมากมีช่วงเวลาสั้น และเรินต์เกนเอง ยังเป็นนักวิทยาศาสตร์คนแรกๆ ที่เป็นผู้นำในการใช้ตะกั่วเป็นโล่ป้องกันอย่างสม่ำเสมอ
การค้นพบเอกซ์เรย์
ในช่วงปี พ.ศ. 2438 เรินต์เกนได้ใช้อุปกรณ์ที่พัฒนาโดยเพื่อนร่วมงานผู้มีชื่อเสียงคือ อีวาน พัลยูอิ (Ivan Palyui) นำมาให้ คือหลอดไฟที่เรียกว่า “หลอดพัลยูอิ” ซึ่งเรินต์เกนพร้อมกับผู้ร่วมงานคนอื่นๆ ได้แก่ ไฮริช รูดอล์ฟ เฮิร์ทซ์, วิลเลียม ครูกส์, นิโค ลา เทสลา และฟิลิบ ฟอน เลนาร์ด ต่างทำการทดลองและทดสอบผลกระทบของการปล่อยประจุไฟฟ้าแรงดึงสูงในหลอดแก้วสูญ ญากาศนี้ จนถึงปลายปี พ.ศ. 2408 บรรดานักค้นคว้าเหล่านี้จึงได้เริ่มทดลองค้นคว้าหาคุณสมบัติของรังสีแคโทด ข้างนอกหลอด ในต้นเดือนพฤศจิกายน เรินต์เกนได้ทดลองซ้ำโดยใช้หลอดของเลนาร์ดโดยทำช่องหน้าต่างด้วยอลูมเนียม บางๆ เพื่อให้รังสีผ่านออกและใช้กระดาษแข็งปิดทับเพื่อป้องกันไม่ให้แผ่น อะลูมิเนียมเสียหายจากไฟฟ้าสถิตย์กำลังแรงที่จะเป็นในการสร้างรังสีแคโทด เรินต์เกนรู้ว่ากระดาษแข็งจะช่วยป้องกันไม่ให้แสงหนีออก แต่เขาได้สังเกตเป็นว่ากระดาษแข็งที่ทาด้วยแบเรียม ปลาติโนไซยาไนด์ (barium platinocyanide) ที่อยู่ใกล้ขอบช่องอะลูมิเนียมเกิดการเรืองแสง เรินต์เกนพบว่าหลอดของครูกส์ที่มีผนังหลอดหนาก็อาจเกิดการเรืองแสงในลักษณะเช่นนี้ได้
ในบ่ายวันที่ 8 พฤศจิกายน พ.ศ. 2438 เรินต์เกนตั้งใจแน่วแน่ว่าจะทดสอบความคิดนี้ เขาได้บรรจงทำแผ่นกระดาษแข็งอย่างระมัดระวังให้เหมือนกับที่ใช้กับหลอดของเล นาร์ด โดยปิดหลอดฮิททอร์ฟ-ครูกส์ด้วยกระดาษแข็งแล้วต่อขั้วจากขดลวดเหนี่ยวนำของ รุห์มคอร์ฟเพื่อสร้างประจุไฟฟ้าสถิตย์ แต่ก่อนที่เรินต์เกนจะตั้งจอที่ทาด้วยแบเรียมปลาติโนไซยาไนด์เพื่อทดสอบความ คิด เขาได้ปิดม่านปิดไฟให้ห้องมืดลงเพื่อดูว่าแผ่นกระดาษแข็งปิดแสงได้มิดหรือ ไม่ ในขณะที่ปล่อยกระแสจากขดลวดเหนี่ยวนำขยับกระดาษแข็งให้แน่นแล้วหันไปเตรียม การขั้นถัดไป เรินต์เกนได้พบว่า ณ จุดนี้เองที่เกิดมีแสงเรืองๆ ขนาดอ่อนๆ ปรากฏที่ปลายโต๊ะที่ห่างออกไป 1 เมตร เพื่อให้แน่ใจ เรินต์เกนได้ปล่อยกระแสจากขดลวดเหนี่ยวนำอีกหลายครั้ง แสงเรืองๆ ก็ยังเกิดขึ้นเหมือนเดิม เขาจุดไม้ขีดไฟดูจึงได้เห็นสิ่งที่อยู่ปลายโต๊ะนั้นแท้จริงก็คือแผ่นกระดาษ แข็งทาสารแบเรียมฯ ที่เตรียมไว้สำหรับการทดลองขั้นต่อไปมั่นเอง
เรินต์เกนคาดเดาว่าสิ่งนี้อาจเกิดจากแสงชนิดใหม่ก็ได้ วันที่ 8 พฤศจิกายน เป็นวันศุกร์ เขาจึงถือโอกาสใช้วันหยุดสุดสัปดาห์ทำการทดลองซ้ำและทำการบันทึกครั้งแรกไว้ ในหลายสัปดาห์ต่อมา เรินต์เกนกินและนอนในห้องทดลองเพื่อทดสอบคุณสมบัติต่างๆ ของแสงชนิดใหม่ที่ยังไม่รู้ว่าเป็นอะไร เขาจึงเรียกชื่อลำลองไปก่อนว่า “รังสี X” เนื่องจากต้องใช้สูตรคณิตศาสตร์กับสิ่ง ที่ยังไม่รู้จักมาก่อน แม้ว่าจะมีผู้เรียกชื่อรังสีนี้ว่า “รังสีเรินต์เกน” เพื่อเป็นเกียรติ แต่ตังเรินต์เกนเองกลับจงใจใช้ชื่อว่า “รังสีเอกซ์” เรื่อยมา
การ ค้นพบรังสีเอกซ์ของเรินต์เกนไม่ใช่อุบัติเหตุ หรือจากการทำงานตามลำพัง ในการเสาะแสวงหาคำตอบ เรินต์เกนและผู้คิดค้นในงานประเภทนี้ในหลายประเทศก็ได้ช่วยกันทำอยู่ การค้นพบเป็นสิ่งที่จะต้องเกิดอย่างเห็นๆ กันอยู่แล้ว ความจริงแล้ว รังสีเอกซ์ได้ถูกสร้างขึ้นและเกิดรูปในฟิล์มแล้วที่มหาวิทยาลัยเพนซิลเวเนีย 2 ปีก่อนหน้านั้น เพียงแต่ว่าคนที่ทดลองทำไม่ได้ตระหนักว่าตนเองได้ค้นพบสิ่งที่ยิ่งใหญ่เข้า แล้ว จึงเก็บฟิล์มเข้าแฟ้มสำหรับใช้อ้างอิงในการทดลองอื่นๆ ในอนาคต ทำให้พลาดในการได้ชื่อว่าตนเป็นผู้ค้นพบสิ่งสำคัญที่สุดทางฟิสิกส์
ณ จุดหนึ่ง ในขณะที่กำลังทดลองขีดความสามารถของวัสดุต่างๆ ในการปิดกั้นรังสี เรินต์เกนได้เอาแผ่นตะกั่วชิ้นเล็กๆ วางขวางทางรังสีได้สังเกตเห็นภาพลางของโครงกระดูกตัวเองปรากฏบนแผ่นจอ แบเรียมฯ ซึ่งเขาได้เขียนรายงานในเวลาต่อมาว่า ตรงจุดนี้เองที่ตนเองตัดสินใจรักษาการทดลองไว้เป็นความลับด้วยเกรงว่าการ ทดลองนี้อาจเกิดจากคลาดเคลื่อนหรือความผิดพลาด
บทความรายงานชิ้นแรกของเรินต์เกน คือ “ว่าด้วยสิ่งใหม่ของรังสีเอกซ์” (On A New Kind Of X-Rays) ตี พิมพ์ใน 50 วันต่อมาคือวันที่ 28 ธันวาคม พ.ศ. 2438 และในวันที่ 5 มกราคม พ.ศ. 2439 หนังสือพิมพ์ของประเทศออสเตรียได้รายงานการค้นพบรังสีชนิดใหม่ของเรินต์เกน เรินต์เกนได้รับปริญญาเอกกิตติมศักดิ์สาขาการแพทย์จากมหาวิทยาลัย เวิร์ซเบิร์กหลังการค้นพบครั้งนี้ เรินต์เกนได้ตีพิมพ์บทความเกี่ยวกับรังสีเอกซ์รวม 3 เรื่อง ระหว่างปี พ.ศ. 2438 - 2440 ข้อสรุปทั้งหมดของเรินต์เกนได้รับการพิสูจน์ว่าถูกต้องทั้งหมด เรินต์เกนได้รับการยกย่องเป็นบิดาแห่งการวินิจฉัยทางรังสีวิทยา เป็นสาขาเชี่ยวชาญเฉพาะที่ใช้ภาพวินิจฉัยโรค
ในปี พ.ศ. 2444 เรินต์เกนได้รับรางวัลโนเบลสาขาฟิสิกส์ซึ่งเป็นรางวัลแรกสุด รางวัลนี้ให้อย่างเป็นทางการเพื่อ “เป็นการรับรู้และยกย่องในความวิริยอุตสาหะที่เขาได้ค้นพบรังสีที่มีความ สำคัญและได้รับการตั้งชื่อตามเขานี้” เรินต์เกนได้บริจาครางวัลทีได้รับให้แก่มหาวิทยาลัยที่เขาสังกัด และได้ทำเช่นเดียวกับที่ ปิแอร์ คูรี ได้ทำบ้างในหลายปีต่อมา คือการปฏิเสธไม่ถือลิขสิทธิ์ในสิ่งประดิษฐ์ต่างๆ ที่สืบเนื่องมาจากผลงานที่เขาค้นพบด้วยเหตูผลทางจริยธรรม เรินต์เกนไม่ยอมแม้แต่จะให้ใช้ชื่อเขาเรียงรังสีที่เขาเป็นผู้ค้นพบ อย่างไรก็ดี ในปี พ.ศ. 2547 IUPAC ได้ตั้งชื่อธาตุใหม่ว่า “เรินต์เกนเนียม” (Roentgenium) เพื่อเป็นเกียรติแก่เรินต์เกน
รังสี...คืออะไร?
รังสี (Radiation) ไม่ใช่ของแปลกใหม่ ไม่ใช่สิ่งประหลาด รังสีเป็นส่วนหนึ่งของธรรมชาติ โดยมาจากการสลายตัวของสารกัมมันตรังสีที่ปะปนในสิ่งแวดล้อมทั่วไป หรือมาจากรังสีที่มีต้นกำเนิดจากภายนอกโลกของเรา รังสีคือพลังงานที่แผ่ออกมาจากต้นกำเนิดในรูปของคลื่นแม่เหล็กไฟฟ้า ได้แก่ คลื่นวิทยุ ไมโครเวฟ แสงสว่าง รังสีเอ็กซ์ และรังสีคอสมิกเป็นต้น และ/หรือ ในลักษณะของอนุภาคที่มีความเร็วสูง เช่น แอลฟา และ เบตา เป็นต้น
รังสี...เกิดขึ้นได้อย่างไร
รังสี ที่เกิดขึ้น ได้ทั้งจากธรรมชาติและการกระทำของมนุษย์ โดยแหล่งที่ก่อให้เกิดรังสีมากที่สุดได้แก่ รังสีจากธรรมชาติ อาทิเช่น จากสารกัมมันตรังสีที่มีในพื้นดินสินแร่และสิ่งแวดล้อม จากอากาศที่เราหายใจ แม้กระทั่งในร่างกายและในอาหารที่เราบริโภค ซึ่งมีการเจือปนด้วยสารกัมมันตรังสีตามธรรมชาติ นอกจากนั้นในห้วงอวกาศก็มีรังสีซึ่งนอกจากรังสีของแสงอาทิตย์แล้ว ก็ยังมีรังสีคอสมิกที่แผ่กระจายอยู่ทั่วจักรวาล แหล่งกำเนิดรังสีที่มาจากการกระทำของมนุษย์มีหลายรูปแบบ อาทิเช่น จากการเดินเครื่องปฏิกรณ์ปรมาณู การระเบิดของระเบิดนิวเคลียร์ รวมทั้งการผลิตสารกัมมันตรังสีจากปฏิกิริยานิวเคลียร์ต่างๆ
รังสีนิวเคลียร์ทั่วไป
รังสีแอลฟา (a) แอลฟาเป็นอนุภาคที่มีคุณสมบัติเหมือนนิวเคลียสของธาตุฮีเลียม (2He4 ) ในแต่ละอนุภาคแอลฟาจะมีประจุไฟฟ้าเป็นบวกสองหน่วย (ประกอบด้วยโปรตอน 2 อนุภาค และ นิวตรอน 2 อนุภาค)
รังสีเบต้า (b) เบ ต้าเป็นอนุภาคที่มีมวลและค่าประจุไฟฟ้าเท่ากับอิเลคตรอน ในแต่ละอนุภาคมีประจุไฟฟ้าหนึ่งหน่วย ถ้าประจุเป็นบวก เรียกว่า อนุภาคเบต้าบวก ( b+ ) หรือ โปสิตรอน หากประจุเป็นลบ เรียกว่าอนุภาคเบตาลบ ( b- ) โดยทั่วๆไปหากเรียกแต่เพียง เบต้า จะหมายถึง อนุภาคเบต้าลบ ทำให้เกิดรังสีในรูปคลื่นแม่เหล็กไฟฟ้าที่เรียกว่า Bremsstrahlung หรือ Braking Radiation ซึ่งมีพลังงานตั้งแต่ 0 ถึงพลังงานสูงสุดของรังสีเบตา และมีอำนาจทะลุทะลวงสูงกว่ารังสีเบตา (วัตถุที่ขวางกั้นรังสีเบตาที่มี Atomic number ต่ำกว่า)
รังสีแกมมา (g) เป็นคลื่นแม่เหล็กไฟฟ้าที่แผ่ออกมาจากนิวเคลียส มีความถี่อยู่ในช่วงประมาณ 1018 ถึง 1021 Hz และมีพลังงานสูง
รังสีเอ็กซ์ (x-rays) เป็น คลื่นแม่เหล็กไฟฟ้าเช่นเดียวกับรังสีแกมมา แต่แผ่ออกมาจากวงโคจรของอิเลคตรอน รังสีเอ็กซ์มีพลังงานต่ำกว่า รังสีแกมมา และมีความถี่อยู่ในช่วงประมาณ 1015 ถึง 1022 Hz รังสีเอ็กซ์มีอยู่สองชนิดได้แก่ Continuous X-rays หรือ Bremsstrahlung และ Characteristic X-rays
รังสีนิวตรอน (n) เป็น อนุภาคที่ไม่มีประจุไฟฟ้า มีอำนาจในการทะลุทะลวงสูง นิวตรอนไม่อาจอยู่อย่างอิสระ จะสลายตัวไปเป็นโปรตรอน อิเลคตรอน และแอนตินิวตริโน ภายในเวลาประมาณสิบสองนาที
กากกัมมันตรังสี...คืออะไร ?
กากกัมมันตรังสีก็คือ ของเสียไม่ว่าในรูปของของแข็ง ของเหลว หรือก๊าซที่ประกอบ หรือปนเปื้อนด้วยสารกัมมันตรังสี ในระดับความแรงรังสีสูงกว่าเกณฑ์กำหนดว่าเป็นอันตราย และวัสดุนั้นๆ ไม่เป็นประโยชน์อีกต่อไปแล้ว เมื่อได้ชื่อว่ากากกัมมันตรังสี กากหรือของเสียเหล่านั้นจะต้องได้รับการบำบัดและจัดการอย่างมีระบบ และผ่านการตรวจสอบอย่างเคร่งครัด
ประเภทของกากกัมมันตรังสี
1. กาก กัมมันตรังสีระดับสูง ได้แก่ กากกัมมันตรังสีที่เป็นของแข็งและของเหลวที่ได้จากการฟอกกากเชื้อเพลิง นิวเคลียร์ และกากกัมมันตรังสีอื่นๆ ที่มีระดับรังสีสูงเทียบเท่า
2. กาก กัมมันตรังสีระดับปานกลาง เป็นกากกัมมันตรังสีที่เกิดจากการปฏิบัติงานที่เกี่ยวข้องกับสาร กัมมันตรังสี อาทิเช่น เศษโลหะ กากตะกอนที่ได้จากการบำบัดกากกัมมันตรังสีที่เป็นของเหลว สารแลกเปลี่ยนไอออน และต้นกำเนิดรังสีใช้แล้ว
3. กาก กัมมันตรังสีระดับต่ำ เป็นกากกัมมันตรังสีที่เกิดจากการปฏิบัติงานที่เกี่ยวข้องกับสาร กัมมันตรังสี อาทิเช่น ถุงมือ เสื้อผ้า อุปกรณ์ที่ทำจากกระดาษ
กากกัมมันตรังสี... ไม่คงอยู่ตลอดไป
สาร กัมมันตรังสีทุกประเภทเป็นสารที่มีการสลายตัว โดยมีช่วงอายุการสลายตัวแตกต่างกัน ตั้งแต่เสี้ยววินาที กระทั่งนับล้านปี ดังนั้นกากกัมมันตรังสีไม่คงอยู่อย่างถาวร พิษของสารรังสีย่อมเจือจางไปตามกาลเวลา โดยที่ช่วงเวลาที่สารรังสีสลายตัวไปครึ่งหนึ่งของปริมาณตั้งต้นเรียก ว่า"ครึ่งชีวิต" โดยทั่วไปแล้วเมื่อทิ้งไว้เพียงช่วงเวลา 10 ช่วงครึ่งชีวิต สารกัมมันตรังสีนั้นๆ ก็จะมีปริมาณความแรงรังสีคงเหลือเพียง 1 ใน 1,000 เท่าของปริมาณตั้งต้น และในช่วงเวลา 20 ช่วงครึ่งชีวิต สารกัมมันตรังสีนั้นจะมีความแรงรังสีเหลือเพียง 1 ใน 1,000,000 เท่าของปริมาณตั้งต้น
กากกัมมันตรังสี...มาจากไหน ?
กากกัมมันตรังสี เกิดขึ้นจากการที่มนุษย์นำเทคโนโลยีนิวเคลียร์มาใช้งานในกิจกรรมต่างๆ เช่น
- การเดินเครื่องโรงไฟฟ้านิวเคลียร์
- การใช้ประโยชน์ในกิจการแพทย์
- การใช้ประโยชน์ในกิจการอุตสาหกรรม
- การใช้ประโยชน์ในกิจการเกษตร
- การใช้ประโยชน์ในการศึกษาวิจัยทางวิชาการต่างๆ
อนึ่ง กากกัมมันตรังสีอาจเกิดขึ้นได้ในกระบวนการนำทรัพยากรแร่ธาตุจากพื้นโลก มาแปรสภาพใช้งานในกิจการต่าง ๆ
กากกัมมันตรังสีจากเครื่องปฏิกรณ์นิวเคลียร์
การ เดินเครื่องปฏิกรณ์นิวเคลียร์ หมายถึง การทำให้เกิดปฏิกิริยานิวเคลียร์ต่อเนื่องตลอดเวลาทำงานและควบคุมได้ ปฏิกิริยานิวเคลียร์ในกรณีของการเดินเครื่องปฏิกรณ์นิวเคลียร์คือ ปฏิกิริยานิวเคลียร์ฟิชชัน ซึ่งคือการที่นิวเคลียสของยูเรเนียม-235 ถูก ทำให้แตกตัว เกิดพลังงานความร้อนและอนุภาคนิวเคลียร์ออกมา พลังความร้อนนั้นเกิดจากการที่มวลสารของเชื้อเพลิงนิวเคลียร์หายไป จึงเกิดพลังงานตามสมการของไอน์สไตน์
E=mc2
E คือ พลังงาน
m คือมวลสาร
c คือความเร็วแสง
ส่วน อนุภาคนิวเคลียร์ที่เกิดขึ้นมีได้หลายอย่าง ที่สำคัญคือ นิวตรอน ซึ่งเกิดจากปฏิกิริยาฟิชชันโดยตรง แต่จะเกิดมีอนุภาคแอลฟา เบต้า และแกมมา ในเครื่องปฏิกรณ์ด้วยจากปฏิกิริยาข้างเคียง ตัวอย่างเช่น เกิดจากการที่นิวตรอนที่เกิดขึ้น วิ่งไปชนวัตถุอื่นๆ ต่อไป หรือเกิดจากการที่ไอโซโทปรังสี ที่มาจากการแตกตัวของยูเรเนียมสลายตัวให้รังสีออกมา การเกิดปฏิกิริยาฟิชชันชนิดต่อเนื่อง (Chain Reaction) จะ เกิดขึ้นเฉพาะที่แกนเครื่องปฏิกรณ์นิวเคลียร์ ซึ่งแท่งเชื้อเพลิงถูกจัดเรียงรวมมัดอยู่อย่างเป็นระเบียบที่ดีเท่านั้น เพราะปฏิกิริยาฟิชชัน จะเกิดขึ้นได้ก็ต่อเมื่อ มีเชื้อเพลิงถึงเกณฑ์วงจรวิกฤต "Critical Mass"
กากกัมมันตรังสีที่เกิดจากการเดินเครื่องปฏิกรณ์นิวเคลียร์ สามารถแยกได้เป็น 2 ส่วน
ส่วนที่หนึ่ง... เกิดจากเนื้อเชื้อเพลิงโดยตรง เนื่องจากเมื่อเกิดปฏิกิริยาฟิชชันขึ้น เชื้อเพลิงนิวเคลียร์ส่วนหนึ่งจะถูกทำปฏิกิริยาหมดไป หรืออีกนัยหนึ่งคือถูก "เผาไหม้" นั่นเอง แต่เชื้อเพลิงใช้แล้ว หรือ "ขี้เถ้า" นั้นจะยังคงอยู่ในแท่งเชื้อเพลิง ซึ่งทำด้วยโลหะคงทน โดยมิได้หลุดรอดออกมาสู่ตัวเครื่องปฏิกรณ์ แท่งเชื้อเพลิงนั้นเราเรียกว่า เชื้อเพลิงใช้แล้ว (Spent Fuel) ขี้เถ้าหรือกาก เชื้อเพลิงในแท่งเชื้อเพลิงใช้แล้วประกอบด้วยสารกัมมันตรังสีหลายชนิด ซึ่งเป็นผลจากปฏิกิริยาฟิชชันที่ทำให้ยูเรเนียมแตกตัวเป็นเสี่ยงๆ แต่ละเสี่ยงหมายถึงธาตุขนาดเล็กลง และมีได้หลายชนิด นอกเหนือจากนั้นในแท่งเชื้อเพลิงใช้แล้ว ยังมีเนื้อยูเรเนียมที่ใช้ไม่หมดอีกจำนวนหนึ่ง และมีธาตุที่หนักกว่ายูเรเนียม ซึ่งเกิดจากปฏิกิริยากระตุ้นด้วยนิวตรอน (Neutron Activation) อีกด้วย ในการเดินเครื่องปฏิกรณ์นิวเคลียร์ผลิตกระแสไฟฟ้า จะมีการเกิดกากกัมมันตรังสีชนิด "เชื้อเพลิงนิวเคลียร์ใช้แล้ว" ประมาณ 1 ใน 3 ของแท่งเชื้อเพลิงทั้งหมดในเครื่องปฏิกรณ์ เช่น หากเป็นโรงไฟฟ้านิวเคลียร์ขนาด 1,000 เมกะวัตต์ จะมีประมาณ 30 ตันต่อปี หรือคิดเป็นปริมาตรได้เท่ากับ 6 ลูกบาศก์ เมตร ซึ่งจะต้องนำเชื้อเพลิงชุดใหม่เข้าไปเปลี่ยน ส่วนแท่งเชื้อเพลิงใช้แล้วที่นำออกมา จะต้องถูกนำเก็บไว้ในสระน้ำ เพื่อลดอุณหภูมิของแท่งเชื้อเพลิงลงชั่วระยะหนึ่ง หลังจากนั้นจึงนำไปเก็บเพื่อบำบัดหรือนำไปทิ้งโดยถาวรต่อไป กากกัมมันตรังสีชนิดนี้ เป็นกลุ่มที่เรียกว่ากากกัมมันตรังสีระดับสูง (High-level Waste)
ส่วนที่สอง... กากกัมมันตรังสีที่เกิดจากส่วนประกอบในการเดินเครื่องปฏิกรณ์ เช่น การใช้เครื่องปฏิกรณ์ต้มน้ำให้ร้อนเป็นไอน้ำ และไอน้ำนั้นไปหมุนปั่นเทอร์ไบน์ผลิตกระแสไฟฟ้า น้ำที่ใช้นั้นอาจมีสิ่งเจือปนอยู่บ้าง สิ่งเจือปนในน้ำที่เข้าไปสู่แกนปฏิกรณ์อาจเกิดปฏิกิริยาจากอนุภาคนิวเคลียร์ ที่เกิดขึ้น ทำให้กลายเป็นสารรังสีซึ่งต้องทำการบำบัด
นอก จากนั้นแล้วยังมีกากกัมมันตรังสีอื่นๆ เช่น ชิ้นส่วนเครื่องปฏิกรณ์ที่ชำรุดต้องเปลี่ยนออก หรือ แม้แต่เสื้อผ้าของผู้ปฏิบัติงานควบคุม หรือเดินเครื่องปฏิกรณ์ เป็นต้น ในโรงไฟฟ้านิวเคลียร์ขนาด 1,000 เมกะวัตต์ จะมีกากกัมมันตรังสีในกลุ่มที่ 2 ซึ่งเรียกว่าเป็น กลุ่มกากกัมมันตรังสีระดับต่ำ (Low level Waste) ประมาณ 100-600 ลูกบาศก์เมตรต่อปี ซึ่งจะมาจาก
- เรซินใช้แล้ว ที่ใช้ในการบำบัดน้ำมีรังสี............................................................225 ลูกบาศก์เมตร
- กากตะกอนจากการต้มระเหยกากฯของเหลว................................................. 300 ลูกบาศก์เมตร
- ขยะต่างๆ รวมทั้งเครื่องกรองอากาศ...............................................................100 ลูกบาศก์เมตร
- อื่นๆ (ชิ้นส่วนอุปกรณ์ที่ชำรุด).......................................................................... 30 ลูกบาศก์เมตร
นอก เหนือจากสองส่วนข้างต้นแล้ว ยังมีกากกัมมันตรังสีจากการทำเหมืองแร่ยูเรเนียม กากกัมมันตรังสีจากการสกัดธาตุยูเรเนียมออกจากสินแร่ และกากกัมมันตรังสีจากการผลิตแท่งเชื้อเพลิงนิวเคลียร์เพื่อใช้งานในโรง ไฟฟ้านิวเคลียร์ รวมกันเรียกว่า เป็นกากกัมมันตรังสีจากวัฏจักรเชื้อเพลิง ซึ่งในกลุ่มนี้มีปริมาณของกากฯ ที่บำบัดแล้วไม่มากนัก
กากกัมมันตรังสีที่เกิดจากการใช้เทคโนโลยีนิวเคลียร์อื่นๆ
ประกอบ ด้วย การใช้สารกัมมันตรังสีปริมาณน้อย โดยใช้เป็นสารเคมีตัวติดตามในขบวนการทางเคมี หรือชีวเคมีต่างๆ สารกัมมันตรังสีชนิดต้นกำเนิดรังสีปิดผนึก ที่มีระดับรังสีตั้งแต่ปริมาณน้อยๆ ใช้ในการตรวจสอบประสิทธิภาพเครื่องมือ การทำงานและการควบคุมคุณภาพของผลิตภัณฑ์อุตสาหกรรมต่างๆ พวกที่มีรังสีระดับปานกลางที่ใช้ในกระบวนการตรวจสอบผลิตภัณฑ์โดยไม่ทำลาย กระทั่งถึงพวกที่มีระดับรังสีสูงมาก ที่ใช้ในการฉายรังสีเพื่อการบำบัดรักษาทางการแพทย์ และการฆ่าเชื้อโรคในอุปกรณ์ผลิตภัณฑ์ทางการแพทย์ และการฉายรังสีเพื่อการถนอมอาหารและผลิตผลการเกษตร เป็นต้น
กาก กัมมันตรังสีอาจเกิดขึ้นได้ในกระบวนการนำทรัพยากรแร่ธาตุจากพื้นโลกมา แปรสภาพใช้งาน วัตถุดิบสำหรับกระบวนการอุตสาหกรรม และเกษตรกรรมหลายอย่างมาจากแร่ธาตุจากพื้นพิภพ ซึ่งในแร่ธาตุจากพื้นพิภพเหล่านั้นจะมีสารกัมมันตรังสีเจือปนอยู่แล้วตาม ธรรมชาติ ดังนั้นเมื่อนำวัตถุดิบต่างๆ ดังกล่าวมาผ่านกระบวนการผลิต ก็จะทำให้เกิดกากกัมมันตรังสีขึ้นได้ ตัวอย่างเช่น การผลิตปุ๋ยฟอสเฟต การสกัดแร่ธาตุหายาก (rare earth mineral) การกลั่น แยกน้ำมันดิบและก๊าซธรรมชาติ โรงไฟฟ้าที่ใช้ถ่านหินและลิกไนต์ เป็นต้น กากกัมมันตรังสีเหล่านี้จัดเป็นพวกที่มีระดับต่ำมาก และได้รับการยกเว้นมิได้ดำเนินการตรวจสอบควบคุม
ข้อมูลกากกัมมันตรังสีในประเทศไทย
ผู้ใช้สารรังสี
ประเภท
|
จำนวน
|
เครื่องปฏิกรณ์ปรมาณูวิจัย
|
1
|
ห้องปฏิบัติการผลิตไอโซโทป
|
1
|
เครื่องเร่งอนุภาคนิวตรอน
|
2
|
เครื่องฉายรังสีแกมมาเพื่อการวิจัย
|
3
|
เครื่องฉายรังสีแกมมาเพื่อการอุตสาหกรรม
|
2
|
อุปกรณ์ฉายรังสีทางการแพทย์
|
20
|
การถ่ายภาพทางรังสีในอุตสาหกรรม
|
12
|
โรงงานที่ใช้สารรังสีในระบบควบคุมการผลิต
|
40
|
ห้องปฏิบัติการวิจัย
|
30
|
โรงงานผลิตนาฬิกา
|
2
|
โรงงานแยกแร่
|
2
|
โรงงานจัดการกากกัมมันตรังสี
|
>1
|
การกระจายและองค์ประกอบของกากกัมมันตรังสีในประเทศไทย
กากกัมมันตรังสี
|
ร้อยละ
|
ไอโซโทปรังสี
|
องค์ประกอบทางเคมี
|
ทางการแพทย์
|
60
|
Ga-67, Cr-51, Tc-99m, I-131,Tl-201, H-3, C-14
|
HCl, Po-34, NO-3, NaCl, NaOH, Serumblood, Scintillants, Urine
|
การศึกษาวิจัย
|
35
|
P-32, S-35, Cr-51, Ca-45, Tc-99m, I-131, Co-60, Cs-137, Am-241, Be-7
|
Po-34, Ca+2, Cl, NO-23, HNO3, H2SO4, HClO4
|
อุตสาหกรรม
|
5
|
Fe-55, Kr-85, Sr-90, Cd-109, Cs-137, Co-60, Ir-192, Am-241, H-3
|
ต้นกำเนิดรังสีชนิดปิดผนึก
|
ประมาณการปริมาณกากกัมมันตรังสีในประเทศไทย
ประเภทของกากกัมมันตรังสี
|
ปริมาณ(ลบ.ม. ต่อปี)
|
ปริมาณรังสี
|
กากกัมมันตรังสีที่เป็นของเหลว (ก่อนบำบัด)
|
200-300
|
40-4,000,000 กิโลเบคเคอเรล/ลบ.เมตร
|
กากกัมมันตรังสีที่เป็นของแข็ง (ก่อนบำบัด)
|
100
|
<10 มิลลิซีเวิร์ต/ชั่วโมง
|
ต้นกำเนิดรังสีปิดผนึก
|
>1
|
>10 มิลลิซีเวิร์ต/ชั่วโมง
|
สารแลกเปลี่ยนไอออนที่ใช้แล้ว
|
2
|
4,000,000 กิโลเบคเคอเรล/ลบ.เมตร
|
แท่งเชื้อเพลิงใช้แล้ว
|
>28 แท่ง
|
รอส่งกลับประเทศผู้ผลิต
|
การจัดการกากกัมมันตรังสี (Radioactive Waste Management)
โดย : ปฐม แหยมเกตุ กองขจัดกากกัมมันตรังสี พปส.
กากกัมมันตรังสี หมายถึง ของเสียทั้งของแข็ง ของเหลวและก๊าซ ที่ประกอบหรือปนเปื้อนด้วยสารกัมมันตรังสีที่ไม่ใช้แล้ว ในระดับกัมมันตภาพรังสีสูงกว่าเกณฑ์ปกติในธรรมชาติ นับตั้งแต่ Henri Becquerel ได้พบกัมมันตภาพรังสีในปี พ.ศ. 2493 เป็นต้นมา ได้มีการศึกษาพัฒนาความรู้และการใช้ประโยชน์ของเทคโนโลยีนิวเคลียร์ต่างๆ มากมาย เช่น การใช้ในรูปของพลังงาน และการใช้สารกัมมันตรังสีในการศึกษาวิจัยและในการปฏิบัติงานอื่น การใช้งานของสารกัมมันตรังสีเพื่อประโยชน์ต่างๆ ดังกล่าว ยังผลให้เกิดกากกัมมันตรังสีขึ้น ผู้ใช้สารกัมมันตรังสีควรต้องทราบถึงกรรมวิธีจัดการกากที่ถูกต้อง เพื่อมิให้เกิดปัญหามลภาวะทางรังสีต่อไป
1) ต้นกำเนิดและลักษณะชนิดของกากกัมมันตรังสี
สารกัมมันตรังสีในกากนั้นอาจจะเป็นสารกัมมันตรังสีตามธรรมชาติ(Natural radioactivity) หรือสารกัมมันตรังสีที่เกิดจากการประดิษฐ์ของมนุษย์ (Artificial radioactivity) การจัดจำพวกของกากกัมมันตรังสีนั้น อาจแยกได้หลายวิธี เช่น
- คุณสมบัติทางเคมี(อินทรีย์สาร อนินทรีย์สาร ฯลฯ)
- ชนิดของสารกัมมันตรังสีที่ปล่อยออกมา(แอลฟา เบตา และ แกมม่า)
- ระดับของการเปรอะเปื้อนสารรังสี(รังสีระดับสูง รังสีระดับต่ำและปานกลาง)
- แหล่งกำเนิดกากฯ หมายถึงสถานที่ปฏิบัติการทางรังสี
2) กากกัมมันตรังสีจากแหล่งกำเนิดกาก
กากกัมมันตรังสีจากขบวนการวัฏจักรเชื้อเพลิงนิวเคลียร์
- กากกัมมันตรังสีจากการทำเหมืองแร่ยูเรเนียม
ปริมาณและคุณภาพของกากกัมมันตรังสีจากเหมืองแร่ยูเรเนียม ขึ้นอยู่กับแหล่งแร่และกรรมวิธีการผลิต โดยปกติกากกัมมันตรังสี ทีเกิดขึ้นคือหางแร่ที่มีระดับรังสีต่ำและสะสมตัวในบ่อน้ำในบริเวณกว้าง ซึ่งไม่เป็นปัญหาสำคัญนัก เพราะแหล่งแร่ยูเรเนียม มักจะอยู่ห่างไกลแหล่งชุมชน สำหรับชนิดของสารกัมมันตรังสีที่พบคือ ยูเรเนียม เรเดียมหรือทอเรียม ที่เจือปนอยู่ในปริมาณเล็กน้อย
- กากกัมมันตรังสีจากการแต่งแร่ยูเรเนียม
สินแร่ยูเรเนียม จะมียูเรเนียมอ๊อกไซด์ U3O8 ประมาณ 0.25% เมื่อส่งออกจากเหมืองแร่ สินแร่ดังกล่าวจะถูกส่งเข้าโรงงานแต่งแร่ ซึ่งจะแยกสารประกอบยูเรเนียม ออกมาจากสิ่งเจือปนทั้งหมดโดยการนำสินแร่มาบดให้แตกละเอียด แล้วสกัดสารประกอบยูเรเนียมออกมาโดยขบวนการทางเคมีซึ่งมี 2 วิธี คือการสกัดโดยกรดและการสกัดด้วยด่าง สารประกอบยูเรเนียมจะละลายในสารละลายและจะถูกนำไปแยกออกจากสารละลาย โดยวิธี Ion Exchange หรือโดยวิธีสกัดด้วยตัวทำละลาย (Solvent Extraction) ต่อไป
กากกัมมันตรังสีจากการแต่งแร่ส่วนใหญ่คือหางแร่ ซึ่งจะเปื้อนปนด้วยสารรังสีที่มาจากการสลายตัวของอนุกรมยูเรเนียม เช่นเดียวกับกากฯ จากเหมืองแร่ กากฯเหล่านี้จะถูกระบายออกสู่บ่อพักและจะตกตะกอนลงสู่ก้นบ่อ โดยจะมีโลหะธาตุอื่นๆปะปนอยู่ด้วย เช่น Mn, Cu, Pb, As ฯลฯ กากกัมมันตรังสีชนิดเดียวกันนี้จะเกิดขึ้นในการแต่งแร่โมนาไซต์ ซึ่งเป็นแร่ที่มีธาตุทอเรียมผสมอยู่ด้วย โดยสรุปแล้วกากกัมมันตรังสีในกลุ่มนี้ไม่ก่อปัญหาสำคัญแต่อย่างใด
- กากกัมมันตรังสีจากขบวนการยูเรเนียมบริสุทธิ์
ผลิตผล จากการแต่งแร่ยูเรเนียม จะได้เป็นสารประกอบยูเรเนียมที่มีเนื้อยูเรเนียมประมาณ 70% ซึ่งจะต้องนำไปทำให้บริสุทธิ์มากยิ่งขึ้น เพื่อให้เหมาะสมต่อการนำไปทำเชื้อเพลิงนิวเคลียร์ต่อไป ทั้งนี้โดยการทำละลายสารประกอบนั้นด้วยกรดดินประสิว แล้วทำการสกัดด้วยสารประกอบ (Tributyl phosphate) ซึ่งจะทำให้สามารถแยกยูเรเนียมเป็นสารประกอบบริสุทธิ์ได้ สำหรับกากกัมมันตรังสีในกรณีนี้ส่วนใหญ่จะอยู่ในรูปของสารละลาย ในปริมาณ 5000 ลิตรต่อยูเรเนียม 1 ตัน กัมมันตภาพรังสีในกากนั้นจะมาจากเรเดียม ยูเรเนียมและผลิตผลจากการสลายตัวของอนุกรมยูเรเนียม เช่น ทอเรียมและโปรเทคติเนียม เป็นต้น หลังจากการสกัดด้วย TBP แล้วจะได้สารประกอบบริสุทธิ์ของ Uranyl Nitrate ซึ่งต่อมาจะถูก Oxidized กลายเป็นก๊าซ Uranium Tetrafluoride ซึ่งจะถูก Reduced ด้วย Mg กลายเป็นโลหะยูเรเนียมบริสุทธิ์ในที่สุด
- กากกัมมันตรังสีจากการประดิษฐ์แท่งเชื้อเพลิงนิวเคลียร์
การ สร้างหรือประกอบแท่งเชื้อเพลิงนิวเคลียร์นั้น จะเกี่ยวกับการนำโลหะยูเรเนียมไปทำเป็นโลหะผสมที่มีความคงทนต่อสภาพต่างๆ อาทิ เช่น ความร้อน ความดัน ความเครียดในแท่งเชื้อเพลิง เป็นต้น การสร้างแท่งเชื้อเพลิงจะต้องอาศัยขบวนการเชิงกล เช่นการหลอมโลหะ การกลึงให้เข้ารูป การเจาะ และการขัดทำความสะอาด เป็นต้น กาก กัมมันตรังสีที่เกิดขึ้น จะประกอบด้วยเศษโลหะ สารละลายที่ใช้ทำความสะอาด กระดาษ ฝุ่นละออง ต่างๆ ซึ่งเศษโลหะจากขบวนการนี้จะถูกเรียกเก็บกลับไปใช้งานใหม่ และกากส่วนอื่นๆนั้นมีระดับรังสีต่ำมาก
- กากกัมมันตรังสีจากการเดินเครื่องปฏิกรณ์ปรมาณู
การเดินเครื่องปฏิกรณ์ปรมาณู จะทำให้เกิดสารกัมมันตรังสีสองจำพวก คือ ผลิตผลของการฟิชชั่น (fission product) และผลิตผลจากปฏิกิริยานิวเคลียร์ระหว่างนิวตรอนกับวัสดุอื่นๆ ในเครื่องปฏิกรณ์ปรมาณู (ผลิตผลแอคติเวชั่น activation products) โดยปกติในส่วนของผลิตผลฟิชชั่นนั้น จะติดค้างอยู่ในแท่งเชื้อเพลิงปรมาณูไม่เล็ดลอดออกมา แต่สำหรับผลิตผลแอคติเวชันนั้นจะปะปนอยู่ในตัวทำความเย็น และวัสดุโครงสร้างอื่นๆของเครื่องปฏิกรณ์ปรมาณู ซึ่งอาจจะถูกชะล้างออกมาในตัวทำความเย็นได้ สารกัมมันตรังสีที่อยู่ในกลุ่มนี้ประกอบด้วยไอโซโทปต่างๆ มากมาย แต่อาจสรุปที่สำคัญได้ดังต่อไปนี้ H3, C14, Fe55, Co60, Ni63, Kr85, Sr89, Sr90, Y91, Zr93, Zr95, Nb95, Tc99, Ru106, I129, I131, Xe133, Cs134, Cs137, Ce141, Ce144, Pm147, SM151, Eu154, PB210, Rn222, Ra226, Th229, Th230, U234, U235, U238, Np237, Pu239, Pu240, PU241, Pu242, Am241, Am243 และ Cm242 เป็นต้น
- กากกัมมันตรังสีจากขบวนการฟอกกากนิวเคลียร์
แท่ง เชื้อเพลิงนิวเคลียร์ที่นำไปใช้งานจนเสื่อมสมรรถนะแล้ว อาจจะนำไปปรุงแต่งให้คืนสภาพใช้งานได้อีกครั้งหนึ่งโดยขบวนการแยกทางเคมี โดยมีวิธีการประกอบด้วย การทำลายแท่งเชื้อเพลิงฯ ด้วยกรดดินปะสิว ซึ่งจะทำให้ได้กากกัมมันตรังสีในรูปของสารละลายที่มีสารกัมมันตรังสีชนิด ผลิตผลฟิชชันที่มีความแรงรังสีสูงมาก โดยปกติผลิตผลฟิชชันนั้นประกอบด้วยธาตุประมาณ 35 ธาตุและเป็นไอโซโทปรังสีประมาณ 120 ชนิด แต่ส่วนใหญ่เป็นไอโซโทปรังสีที่มีอายุสั้นๆ สำหรับผลิตผลฟิชชันที่มีครึ่งชีวิตยาวมีไม่มากนัก ที่สำคัญคือ Cs137 มีครึ่งชีวิต 30 ปี Sr90มีครึ่งชีวิต 29 ปีและ Ru106 มีครึ่งชีวิต 1 ปี เป็นต้น นอกจากผลิตผลฟิชชันแล้ว กากกัมมันตรังสีชุดนี้ยังประกอบด้วยสารรังสีชนิดทรานสยูเรนิค (Transurenic) ซึ่งเป็นไอโซโทปรังสีของธาตุที่มีเลขอะตอมสูงกว่ายูเรเนียม และเป็นไอโซโทปที่ให้แอลฟาเป็นส่วนใหญ่ และมีครึ่งอายุค่อนข้างยาวนานด้วย
- กากกัมมันตรังสีจากศูนย์วิจัยฯ และสถาบันการศึกษา
กัมมันตภาพ รังสีของกากฯ ในกลุ่มนี้มีระดับรังสีต่ำมาก แต่ปรากฏว่าปริมาณของกากรังสีเพิ่มมากขึ้นทุกที เนื่องจากปัจจุบันมีการใช้สารรังสีในการศึกษาวิจัยในโครงการต่างๆ เพิ่มมากขึ้น กากกัมมันตรังสีในกลุ่มนี้มีสภาพทางกายภาพคล้ายคลึงกัน แต่องค์ประกอบของกากแตกต่างกัน ขึ้นกับโครงงานที่ปฏิบัติ อาทิเช่น กากของเหลวอาจเป็นพวกสารอนินทรีย์ที่มีการเจือปนด้วยสารเคมีต่างชนิดกัน หรืออาจเป็นสารละลายอินทรีย์ชนิดต่างๆ เป็นต้น สำหรับกากของแข็งนั้น ส่วนมากประกอบด้วยวัสดุอุปกรณ์ที่ชำรุด หรือเศษกระดาษ ผ้า เฟอร์นิเจอร์ ขวดแก้ว พลาสติก และอื่นๆ
- กากกัมมันตรังสีที่มาจากการใช้งานทางการแพทย์
การ ใช้ประโยชน์ทางรังสีในกิจการแพทย์ประกอบด้วย การใช้ในการตรวจวินิจฉัยและการบำบัดรักษาอาการโรค เช่น การใช้สารรังสีฉีดเข้าไปในร่างกาย และตรวจสอบการทำงานของระบบอวัยวะต่างๆ โดยการติดตามวัดปริมาณรังสี การใช้รังสีจากต้นกำเนิดรังสีฉายไปยังบริเวณอวัยวะที่เป็นเนื้องอก เพื่อระงับการแพร่ขยายของเนื้อร้าย ณ อวัยวะส่วนนั้น และการใช้รังสี X ฉายผ่านอวัยวะของร่างกาย เพื่อตรวจหาความผิดปกติ เป็นต้น ทั้งนี้สารรังสีที่ใช้มีทั้งในลักษณะของต้นกำเนิดรังสีผนึกสนิท (sealed source) และสารเคมีรังสีชนิดไม่ผนึก(unsealed sources) กาก กัมมันตรังสีที่เกิดขึ้น อาจจะอยู่ในรูปของเสียที่ขับถ่ายจากผู้ป่วยที่ได้รับสารรังสีเข้าสู่ร่างกาย น้ำเสียจากการทำความสะอาดภาชนะหรือเครื่องแต่งกายของผู้ป่วย และภาชนะบรรจุสารกัมมันตรังสี เข็มฉีดยาและอื่นๆ สารรังสีที่ใช้ในกิจการนี้มักเป็นพวกที่มีครึ่งอายุสั้นๆเช่น Au198, I125, Cr51 และ Tc99m เป็นต้น
- กากกัมมันตรังสีจากโรงงานอุตสาหกรรม
ปกติ สารกัมมันตรังสีที่ใช้ในกิจการอุตสาหกรรมต่างๆ นั้น มักอยู่ในสภาพของสารรังสีชนิดผนึกสนิทในภาชนะ (seal source) โดยส่วนมากจะมีการใช้งานในการถ่ายภาพทางรังสี (radiography) ของชิ้นส่วนอุปกรณ์ต่างๆ หรือเครื่องยนต์กลไก การใช้เป็นเครื่องตรวจสอบความหนาของวัสดุ ตรวจสอบความหนาแน่น ตรวจสอบระดับของเหลวในถังทึบ เป็นต้น ต้นกำเนิดรังสีเหล่านั้นจะถูกเรียกว่ากากกัมมันตรังสีก้ต่อเมื่อเลิกใช้งาน แล้ว ซึ่งในเวลานั้นสารรังสีจะมีความเข้มของรังสีลดลงอย่างมากแล้ว และเป็นกากที่แยกจากองค์ประกอบอื่นๆ ได้ง่าย ตัวอย่างไอโซโทปรังสีในกรณีนี้ เช่น โคบอลต์-60 เออริเดียม-192 ซีเซียม-137 เป็นต้น
- กากกัมมันตรังสีจากการใช้งานทางการเกษตร
การ ศึกษาวิจัยทางการเกษตรหลายอย่าง เป็นต้นกำเนิดกากกัมมันตรังสีประเภทนี้ อาทิเช่น การตรวจสอบสภาพดิน หรือการศึกษาความสามารถในการดูดซึมปุ๋ยของพืชชนิดต่างๆ การตรวจหาความชื้นใต้ดิน ฯลฯ กากกัมมันตรังสีที่เกิดขึ้นมักจะมีลักษณะเช่นเดียวกับกากที่เกิดจากศูนย์ วิจัยนิวเคลียร์ทั่วไป
3) หลักการจัดการกากกัมมันตรังสี
การ ขจัดกากกัมมันตรังสี มิได้หมายถึงการทำลายสารกัมมันตรังสีให้หมดสิ้นไป ทั้งนี้เพราะวิธีการทางเคมี-ฟิสิกส์สามัญ ไม่สามารถทำลายสภาพกัมมันตรังสีได้ จะมีเพียงวิธีทางนิวเคลียร์ซึ่งยุ่งยากและสิ้นเปลือง และขบวนการสลายตัวตามธรรมชาติของสารกัมมันตรังสีนั้นเท่านั้น ที่จะแปรสภาพความเป็นกัมมันตภาพรังสีของสารได้ การจัดการกากกัมมันตรังสีจึงเป็นการดำเนินการใดๆ เพื่อป้องกันการแพร่กระจายของกากกัมมันตรังสีในสภาวะแวดล้อม เกิดการเปรอะเปื้อนด้วยสารกัมมันตรังสี ซึ่งอาจก่อให้เกิดผลกระทบต่อสุขภาพของประชาชนโดยทั่วไป
วิธี การที่ใช้ปฏิบัติต่อกากฯ เหล่านั้นมีมากมายหลายวิธี ตามลักษณะคุณภาพและปริมาณของกากฯ เหล่านั้น แต่โดยส่วนมากแล้วการขจัดกากฯ ทุกๆ วิธีจะมีหลักการร่วมกัน 3 ประการ คือ
3.1. การทำให้เข้มข้น แล้วเก็บรวบรวม ( concentrate and contain )
3.2. การทำให้เจือจาง แล้วระบายทิ้ง ( dilute and disperse )
3.3. การเก็บทอดระยะเวลา และปล่อยให้สารกัมมันตรังสีสลายตัวไปเอง ( Delay and Decay )
4) การขจัดการของเหลวกัมมันตรังสี
- กากของเหลวระดับรังสีสูง (104 – 106 Ci/m3)
กากกัมมันตรังสีชุดนี้ ส่วนใหญ่เป็นสารละลายของ fission – product จากโรงงานคืนสภาพเชื้อเพลิงนิวเคลียร์ และมีระดับรังสีสูง การบำบัดกากนี้ มักใช้วิธีการต้มระเหย (evaporation) แล้วเก็บไว้ในภาชนะที่คงทน รอจนสารรังสีบางส่วนสลายตัวลงบ้าง แล้วจึงนำไปทำเป็นผลิตภัณฑ์ของแข็ง เช่นโดยวิธีผนึกให้เป็นแก้ว ( Vitrification) ต่อไป
- กากของเหลวระดับรังสีต่ำและปานกลาง (10-6 – 1 Ci/m3)
ตาม ปกติ กากของเหลวกัมมันตรังสีมักจะอยู่ในรูปสารละลายของน้ำ เพราะน้ำเป็นองค์ประกอบสำคัญในการปฏิบัติงานทุกประเภท เช่น ใช้น้ำทำความสะอาดอุปกรณ์ ใช้ทำละลายสารเคมีต่างๆ ในห้องปฏิบัติการ การดำเนินการขจัดกากของเหลวกัมมันตรังสีนั้น จะเริ่มด้วยการรวบรวมกากของเหลวไว้จนกระทั่งมีปริมาณมากพอ ซึ่งจะได้ประโยชน์สองประการคือ เป็นการทอดระยะเวลาให้สารกัมมันตรังสีที่มีอายุสั้นๆ สลายตัวหมดไป (ตามหลักการข้อที่3) และเป็นการประหยัดค่าใช้จ่าย เพราะสามารถดำเนินการต่อกากฯ จำนวนพอเหมาะ ในการเดินเครื่องครั้งหนึ่งๆ วิธีการดำเนินการขจัดกากของเหลวมีหลายวิธี เช่น
การตกตะกอนเคมี เป็น วิธีที่ใช้สารเคมีผสมลงในของเหลวฯ ทำให้สารกัมมันตรังสีเกิดการตกตะกอนร่วมกับสารเคมีนั้น (หลักการข้อที่1) และสารละลายในส่วนที่เหลือหลังจากเกิดการตกตะกอน จะถูกระบายทิ้งต่อไป (หลักการข้อที่2)
ผลจากวิธีทางเคมี คือการเกิดสารประกอบที่ไม่ละลายน้ำซึ่งมักเป็นเกลือ hydroxide carbonate หรือ phosphate ขึ้นกับวิธีการและสารเคมีที่ใช้งาน
การต้มระเหย (Evaporation) เป็นวิธีที่ใช้ความร้อนในการต้มระเหยน้ำทิ้งกัมมันตรังสี โดยเฉพาะอย่างยิ่งพวกที่มีระดับรังสีปานกลาง กรรมวิธีนี้จะทำให้ค่า DF สูงมาก การต้มระเหยนี้จะได้ผลเป็นกากกัมมันตรังสีที่เข้มข้นในรูปตะกอน หรือของเหลวข้นๆ (concentrated residue) ตามหลักการข้อที่ 1 และส่วนที่เป็นไอน้ำ (Distillate) จะถูกระบายออกไป ตามหลักการข้อที่ 2
การดูดจับด้วยสารแลกเปลี่ยนไอออน (Ion Exchange) เนื่อง จากสารกัมมันตรังสีในกากของเหลวฯ จะอยู่ในรูปอนุมูลของธาตุด้วย ดังนั้นจึงสามารถใช้วิธีแลกเปลี่ยนไอออนในการขจัดกากของเหลวฯ ได้ โดยให้กากของเหลวไหลผ่านคอลัมน์ของสารแลกเปลี่ยนไอออนซึ่งอาจเป็นสาร สังเคราะห์ เช่น Ion Exchange resin หรือสารที่มีกำเนิดแต่ธรรมชาติ เช่น ถ่าน เกลือ ซีโอไลต์ เบนโตไนท์ และ ดินเคลย์ ต่างๆ สารกัมมันตรังสีจะถูกดุดจับไว้ในสารแลกเปลี่ยนไอออน (หลักข้อที่ 1) และสารละลายที่ผ่านออกไปสามารถละลายทิ้งได้ (หลักข้อที่ 2)
สำหรับการปฏิบัติงานขจัดกากของเหลวกัมมันตรังสีของสำนักงาน พปส. นั้นกระทำโดยใช้วิธีตกตะกอนเคมี
5) การขจัดกากของแข็งกัมมันตรังสี
กากกัมมันตรังสีระดับรังสีสูง กากของแข็งชุดนี้ได้จากโรงงานคืนสภาพเชื้อเพลิงนิวเคลียร์ (nuclear fuel reprocessing plant) ลักษณะของกากคือ อ๊อกไซด์ของธาตุต่างๆ การบำบัดกากฯ จะกระทำโดยแปรสภาพของกากให้เป็นวัสดุที่คงทนต่อปฏิกิริยาเคมี อาทิเช่น แก้ว หรือ เซรามิค กากของแข็งที่แปรสภาพแล้ว เรียกว่า ผลิตภัณฑ์กากฯ (Waste product) จะถูกบรรจุลงในภาชนะที่เหมาะสม และเก็บไว้รอการทิ้งกากโดยถาวรต่อไป
กากกัมมันตรังสีระดับรังสีต่ำและปานกลาง กากของแข็งในกลุ่มนี้ ประกอบด้วย
- กากตะกอนเข้มข้น(Residue) จากการต้มระเหยกากของเหลวจากขบวนการตกตะกอนเคมีของกากของเหลว และ/หรือ จากสารแลกเปลี่ยนไอออนที่ใช้แล้ว เป็นต้น กากตะกอนเหล่านี้มักจะมีความชื้นปะปนอยู่ด้วย และยังไม่คงทนต่อสภาวะแวดล้อม ดังนั้นจะต้องมีการแปรสภาพเป็นผลิตภัณฑ์กากที่เหมาะสมเช่นกัน การแปรสภาพกากดังกล่าวนี้ อาจกระทำได้โดยวิธี Cementation หรือวิธี Bituminization
- กากของแข็งจากการใช้งานทั่วไป กากของแข็งกัมมันตรังสีส่วนใหญ่ มาจากอุปกรณ์ที่ใช้ปฏิบัติงานทางรังสี เช่น ภาชนะต่างๆ เศษกระดาษ และซากสัตว์ทดลอง เป็นต้น วิธีการปฏิบัติต่อกากกลุ่มนี้ก็คือ ลดปริมาตรของกากฯ และเก็บรวบรวมไว้ การลดปริมาตรของกากฯ สามารถกระทำได้เช่น
- การเผาทำลายกากฯที่เผาไหม้ได้ (Incineration)
- การกด / อัดกากฯ ด้วยเครื่องมืออัดกำลัง (Compaction)
- การบด / ตัดกากฯ ที่มีขนาดใหญ่ให้มีขนาดเล็กลง (Fragmentation)
- การหลอมละลายโลหะเปื้อนรังสี (Melting)
- การทำละลายด้วยกรด (Acid reduction)
กาก ของแข็งที่ทำการลดปริมาตรลงแล้ว จะเก็บรวบรวมไว้และนำไปแปรสภาพให้เหมาะสม เพื่อนำไปเก็บหรือทิ้งลงสู่สิ่งแวดล้อมตามธรรมชาติ โดยไม่ก่อให้เกิดมลภาวะทางรังสีต่อสภาวะแวดล้อม
6) การขจัดกากกัมมันตรังสีชนิดที่เป็นไอหรือก๊าซ
กากกัมมันตรังสีที่อยู่ในสถานะของก๊าซนั้นมีอยู่ 2 ลักษณะได้แก่ ก๊าซกัมมันตภาพรังสี (radioactive gas) เช่น I2, Kr, Ar, Rn และ Xe เป็นต้น หรือ ไอสาร หรือ ฝุ่นละอองที่ปนเปื้อนด้วยสารกัมมันตรังสี (Aerosols) การบำบัดกากฯ ชนิด Aerosols นั้นกระทำได้โดยวิธีกรองกากฯ ในอากาศด้วยระบบกรองพิเศษ ซึ่งมักจะประกอบด้วย Activated Charcoal เป็นตัวดูดจับสารกัมมันตรังสี และมีอุปกรณ์กรองมวลสารแขวนลอยที่มีขนาดเล็กๆ ได้ดี HEPA filter จากการขจัดกากฯ โดยการกรองแล้ว เครื่องกรองจะถูกทิ้งเป็นกากของแข็งต่อไป
การบำบัดกากชนิดที่เป็นก๊าซกัมมันตรังสีนั้นจำเป็นต้องอาศัยกรรมวิธีเฉพาะ เช่น
- เทคนิคการดูดจับ (Adsorption technique) ได้แก่การดูดจับก๊าซกัมมันตรังสีด้วยสารตัวกลางที่เหมาะสม เช่น Activated Carbon หรือ Porous matter ที่เคลือบหรือจุ่มให้โชกด้วยเกลือของเงิน (Silver Nitrate Impregnated) ในกรณีของ I2
- การสกัดแยก (Extraction) เช่น การสกัดแยกด้วยวิธีกลั่นเย็น (Cryogenic distillation) ซึ่งกระทำได้โดยการลดอุณหภูมิของก๊าซให้เย็นจัดจนกลายเป็นของเหลว แล้วปล่อยให้อุณหภูมิสูงขึ้นทีละน้อย ก๊าซแต่ละชนิดที่มีจุดเดือดแตกต่างกันก็จะระเหยออกมา ณ ที่อุณหภูมิต่างกัน ตัวอย่างเช่น Ne มีจุดเดือด = -111.9oC เป็นต้น
- การแพร่ (Diffusion) เป็นการสกัดแยกก๊าซอีกแบบหนึ่งโดยอาศัยหลักการที่ว่า ก๊าซแต่ละชนิดมีอัตราการแพร่ (rate of diffusion) ในตัวกลางต่างๆ ไม่เท่ากัน ดังนั้นจึงสามารถแยกจากกันได้
หลัง จากการกรองหรือสกัดแยกก๊าซด้วยวิธีต่างๆ ดังกล่าวแล้ว ชุดเครื่องกรองก็จะเป็นที่สะสมของสารกัมมันตรังสี และจะต้องนำไปบำบัดเป็นกากของแข็งต่อไป ส่วนก๊าซที่สกัดแยกเอาไว้ก็บรรจุใส่ท่อหรือถังก๊าซ เพื่อนำไปทิ้งโดยถาวรต่อไป
7) การแปรสภาพของแข็งให้เหมาะต่อการเก็บทิ้งโดยถาวร (Conditioning)
เพื่อทำให้สภาพของกากฯ คงทนต่อสภาพแวดล้อม ในเมื่อจะมีการเก็บทิ้งโดยถาวรจะต้องมีการแปรสภาพกากฯ เช่น การผนึกกากฯ ในเนื้อซีเมนต์ (cementation) โดย ใช้ซีเมนต์เป็นตัวยึด/เชื่อมกากกัมมันตรังสี และป้องกันไม่ให้สารกัมมันตรังสีในกากฯ กระจายออกสู่สภาวะสิ่งแวดล้อม หรืออาจจะผนึกกากฯ ในสารบิทูเมน หรือยางมะตอย (bituminization) หรืออาจจะแปรสภาพของกากฯ ให้อยู่ในรูปของสารที่เสถียรมากๆ เช่น แก้วและเซรามิค (Vitrification) เป็นต้น การเลือกวิธีแปรสภาพนั้นขึ้นอยู่กับชนิดและองค์ประกอบของกากฯ นั้นๆ และเหตุผลทางเศรษฐกิจของการจักการกากนั้นๆ
8) การเก็บรักษาและทิ้งกากโดยถาวร
กากฯ ที่แปรสภาพแล้ว สามารถนำไปทิ้งโดยถาวรได้ ซึ่งมีวิธีทิ้งหลายวิธี เช่น การเก็บฝังลงใต้ดินตื้นๆ การเก็บฝังในเหมืองแร่ร้างใต้ดินและการเก็บทิ้งลงในมหาสมุทร เป็นต้น
การทิ้งกากแบบฝังดิน สามารถกระทำได้ 2 วิธี
- การทิ้งกากแบบฝังดิน (Shallow land burial) เป็น วิธีการที่ใช้กับกากกัมมันตรังสีของแข็ง ที่มีความแรงรังสีต่ำ และมีครึ่งชีวิตของสารกัมมันตรังสีสั้น (ไม่เกิน 30 ปี) ที่ฝังกากแบบนี้อาจเป็นหลุมดินหรือเป็นบ่อที่มีโครงสร้างแข็งแรง (engineered structure)
- การทิ้งกากแบบฝังดินลึก (Deep underground disposal) เป็น การทิ้งกากที่เหมาะสมสำหรับกากกัมมันตรังสีที่มีครึ่งชีวิตยาว และมีระดับความแรงรังสีสูง และต้องการแยกกากจากมนุษย์และสิ่งแวดล้อมที่เกี่ยวข้องกับประชาชนให้มากที่ สุด
การทิ้งกากแบบทิ้งทะเล
การ ทิ้งกากแบบนี้ อาจกระทำได้โดยการทิ้งผลิตภัณฑ์กากที่ผนึกสนิทแล้วลงสู่ท้องทะเลโดยตรง หรือโดยวิธีฝังกากใต้ดินใต้ท้องทะเลลึกแต่จะต้องปฏิบัติตามกฏเกณฑ์ข้อตกลง นานาชาติ ว่าด้วยการทิ้งกากสารอันตรายลงสู่ท้องทะเล (The London Dumping Convention) ปัจจุบันนี้ประเทศต่างๆทั่วโลกพยายามละเว้นการทิ้งกากวิธีนี้
การทิ้ง/ทำลายกากโดยถาวรวิธีอื่นๆ
ยังมีวิธีทำลายกากอีกหลายวิธี ที่มีการพิจารณาว่าอาจจะนำมาใช้ปฏิบัติได้ ตัวอย่างเช่น การฝังกากลงในน้ำแข็ง (disposal into ice sheet) การทำลายกากโดยวิธีนิวเคลียร์ (Nuclear transmutation) และการทิ้งกากออกไปสู่อวกาศ (disposal into space) เป็นต้น อย่างไรก็ตามเทคนิคการทิ้งกากด้วยวิธีดังกล่าว ยังมิได้นำมาใช้ปฏิบัติในปัจจุบัน
การป้องกันอันตรายจากรังสี
การป้องกันอันตรายจากรังสี จะประสบความสำเร็จตามเป้าหมายได้ ขึ้นอยู่กับการบริหารองค์กรความปลอดภัย (Safety organization) ให้ มีประสิทธิภาพสูง และประกอบกับผู้ปฏิบัติงานทางรังสีในหน่วยงานนั้น ตลอดจนผู้บังคับบัญชาที่รับผิดชอบ จะต้องร่วมมือกัน ให้การสนับสนุน และให้ความสนใจอย่างต่อเนื่อง ตลอดจนติดตามการจัดการในทุกระดับชั้นอย่างระมัดระวัง โดยอาศัยมาตรการต่างๆ ดังต่อไปนี้
1. การประเมินอันตราย (Hazard evaluation)
การ ประเมินอันตรายเป็นขั้นตอนสำคัญ ในการกำหนดโครงการความปลอดภัยทางรังสี เราจะต้องทราบความเป็นมาและขอบเขตของอันตรายที่จะเกิดขึ้นต่อสุขภาพ ในการปฏิบัติการใดๆ เกี่ยวกับต้นกำเนิดรังสี บนรากฐานเกี่ยวกับการประเมินอันตรายจากรังสีนี้ สถานที่ปฏิบัติการทางรังสี จะต้องมีการวางแผนการป้องกันอันตรายจากรังสีเป็นอย่างดี ตลอดจนวางระเบียบปฏิบัติในการทำงานเกี่ยวกับสารรังสี เพื่อให้แน่ใจได้ว่าระดับของปริมาณรังสี (Radiation dose) และ ความเข้มข้นของสารรังสีที่ปนเปื้อนอยู่ในอากาศและในน้ำอยู่ในระดับต่ำที่สุด เท่าที่จะเป็นไปได้ และไม่ว่าในกรณีใดๆ จะไม่เกินค่าสูงสุดที่ยอมรับได้ (Maximum permissible values) ซึ่งกำหนดโดยคณะกรรมาธิการนานาชาติ ว่าด้วยการป้องกันอันตรายจากรังสี (International Commission on Radiological Protection, ICRP) ได้ มีการประชุมปรึกษาหารือ และทบทวนปรับปรุงระดับค่าต่างๆ ของวัสดุกัมมันตรังสีในน้ำและอากาศอยู่เสมอเป็นระยะๆ ความเจริญก้าวหน้าของวิชาการต่างๆ และข้อมูลใหม่ๆ ที่ได้รับมา ค่าต่างๆ เหล่านี้ได้มีการกำหนดค่าไว้สำหรับกลุ่มบุคคลสองกลุ่ม คือผู้ปฏิบัติงานเกี่ยวข้องกับสารรังสี และประชาชนทั่วไป โดยถือว่าถ้าร่างกายของคนทั้งสองกลุ่มนี้ได้รับรังสี หรือวัสดุกัมมันตรังสีเข้าไป ไม่เกินค่าที่ ICRP กำหนด ไว้สำหรับธาตุทางรังสีแต่ละตัวแล้ว ความเสี่ยงอันตรายต่อภัยทางรังสี หรือความเสียหายที่จะเกิดขึ้นต่อสุขภาพของบุคคลนั้น ถือว่าอยู่ในเกณฑ์ที่ยอมรับกันได้ และได้นำค่าตัวเลขเหล่านี้มาใช้เป็นข้อมูลขั้นพื้นฐาน ในการออกแบบสถานที่ปฏิบัติการทางรังสี การพัฒนาระเบียบปฏิบัติการที่เหมาะสม อย่างไรก็ตาม ICRP ยังได้แนะนำว่า การได้รับรังสีทั้งหลายควรจะรักษาให้อยู่ในขีดจำกัดต่ำที่สุดเท่าที่จะเป็น ไปได้ ในขณะที่ระดับรังสีสูงสุดอันเป็นที่ยอมรับกันได้ สามารถใช้เป็นแนวทางในการวางแผน แต่ไม่ควรถือว่าเป็นระดับที่ผู้ปฏิบัติงานทางรังสีสามารถรับได้เป็นประจำ ซึ่งผิดเจตนารมณ์ที่แท้จริง ในทางปฏิบัติแล้วผู้ปฏิบัติงานทางรังสีจะต้องพยายามให้ตัวเองและผู้อื่นได้ รับรังสี น้อยที่สุดเท่าที่จะเป็นไปได้
เพื่อหลีกเลี่ยงปัญหาข้อโต้แย้งในทางกฎหมาย การใช้คำว่าระดับสูงสุดที่อนุญาตให้รับได้ (Maximum permissible levels) นั้น ประกอบกับปัญหาในแง่ของจิตวิทยาแล้ว ถ้าใครได้รับรับรังสีมีค่าเกินค่าที่ ICRP ได้ กำหนดไว้ จะต้องอยู่ในสภาวะที่เป็นอันตราย ซึ่งจะไม่เป็นความจริง ดังนั้นในการยกร่างเกี่ยวกับแนวปฏิบัติทางกฎหมาย ให้เลี่ยงไปใช้คำว่า ขีดจำกัดในการปฏิบัติการหรือปริมาณรังสีอันเป็นที่ยอมรับได้ (Operational limits or acceptable dose) แทน ดูจะเหมาะสมกว่า
2. การออกแบบสถานที่ปฏิบัติการหรืออุปกรณ์ (Design of installations or devices)
ใน การออกแบบสถานที่ปฏิบัติการหรืออุปกรณ์ สำหรับใช้เกี่ยวกับต้นกำเนิดรังสีด้วยความระมัดระวัง ก็เป็นอีกขั้นตอนหนึ่งที่สำคัญ ในการ ป้องกันอันตรายจากรังสี โดยให้มีการผนวกเอาระบบของความปลอดภัย และการป้องกันอันตรายจากรังสีเข้าไว้ในแผน การออกแบบก่อสร้างสถานปฏิบัติการหรืออุปกรณ์ อันเป็นการลดอิทธิพลความผิดพลาดที่อาจจะเกิดขึ้นจากความผิดพลาดที่มนุษย์ เป็นผู้ก่อขึ้น ทำให้มีโอกาสได้รับรังสีจากการปฏิบัติงานสูงกว่าปกติ ระบบของความปลอดภัยที่จะใช้ในการออกแบบจะมากหรือน้อย ก็ขึ้นกับลักษณะของงาน ที่ทำ เช่น ถ้า ในกรณีที่มีการใช้ต้นกำเนิดรังสีที่มีความแรงรังสีสูงมากในทางการแพทย์ หรืออุตสาหกรรม ระบบของความปลอดภัยก็ย่อมต้องมีสูงตามไปด้วย และจะลดระดับลงถ้าใช้ต้นกำเนิดรังสีที่มีความแรงรังสีต่ำลงมา ดังนั้นจึงต้องมีการยกร่างระเบียบปฏิบัติอย่างระมัดระวัง และการควบคุมทางการบริหารที่เหมาะสมควบคู่กันไปด้วย
การ ออกแบบสถานที่ปฏิบัติการ รวมทั้งทำเลที่ตั้ง การวางผัง และการกำบังรังสีพื้นที่บริเวณสถานที่ปฏิบัติงาน ในการที่จะบรรลุการออก แบบที่เหมาะสม จะต้องมีการพิจารณาถึงองค์ประกอบอื่นๆ อีกหลายองค์ประกอบ รวมทั้งประเภทและความแรงของต้นกำเนิดรังสีที่จะใช้ในระยะแรก และเผื่อไว้สำหรับในอนาคตที่อาจจะมีการขยายการใช้เพิ่มขึ้นด้วย
หลักสามประการในการป้องกันอันตรายจากรังสีคือ
- 1) เวลา การปฏิบัติงานทางด้านรังสีต้องใช้เวลาน้อยที่สุด เพื่อป้องกันมิให้ร่างกายได้รับรังสีเกินมาตรฐานที่กำหนดไว้สำหรับบุคคล
- 2) ระยะทาง ความ เข้มของรังสีจะเปลี่ยนแปลงลดลงไปตามระยะทางจากสารต้นกำเนิดรังสี สำหรับต้นกำเนิดรังสีที่เป็นจุดเล็กๆ ความเข้มจะลดลงเป็นสัดส่วนกลับกับระยะทางยกกำลังสอง
- 3) เครื่องกำบัง ความเข้มของรังสีเมื่อผ่านเครื่องกำบังจะลดลง แต่จะมากหรือน้อย ขึ้นอยู่กับพลังงานของรังสี คุณสมบัติ ความหนาแน่น และ ความหนาของวัตถุที่ใช้
เครื่องวัดรังสี
เครื่องวัดรังสีที่นิยมใช้กันโดยทั่วไปได้แก่ เครื่องสำรวจรังสี เครื่องบันทึกรังสีประจำตัวบุคคล เครื่องวัดรังสีประจำตัวบุคคลชนิดเตือนภัย และเครื่องตรวจวัดรังสีประจำที่
เครื่องสำรวจรังสี
เป็นเครื่องตรวจหารังสีที่ใช้แบตเตอรี สะดวกต่อการพกพา เช่น Geiger Muller และ Ionization Chamber
เครื่องบันทึกรังสีประจำตัวบุคคล
เป็นเครื่องมือบันทึกปริมาณรังสีที่ร่างกายได้รับ ซึ่งเจ้าหน้าที่ที่ปฏิบัติงานด้านรังสีจำเป็นต้องพกติดตัว มีหลายชนิด เช่น pocket dosimeter, film badge, thermoluminescent dosimeter (TLD)
เครื่องวัดรังสีประจำตัวบุคคลแบบเตือนภัย
เป็นเครื่องวัดสำหรับพกพาติดตัว จะส่งเสียงหรือแสง เพื่อเตือนให้ทราบเมื่อระดับรังสีสูงเกินกว่าที่กำหนดไว้ในเครื่อง
เครื่องตรวจรังสีประจำที่
เป็นเครื่องวัดรังสีชนิดติดตั้งประจำที่ เมื่อตรวจพบรังสีที่สูงกว่าค่าที่กำหนดไว้จะส่งเสียงและแสงเตือน
การสลายตัวของธาตุกัมมันตรังสี
การที่ธาตุกัมมันตรังสีแผ่รังสีได้นั้นเป็นเพราะนิวเคลียสของธาตุไม่เสถียร เนื่องจากมีพลังงานส่วนเกินอยู่ภายใน ดังนั้นจึงจำเป็นต้องถ่ายเทพพลังงานส่วนเกินนี้ออกไป เพื่อให้นิวเคลียสเสถียรในที่สุด พลังงานส่วนเกินที่ปล่อยออกมาอยู่ในรูปของอนุภาคหรือรังสีต่าง ๆ เช่น อนุภาคแอลฟา อนุภาคบีตา รังสีแกมมาและไอโชโทปที่เสถียร จากการศึกษาไอโชโทปของธาตุจำนวนมาก พบว่าไอโชโทปที่นิวเคลียสมีอัตราส่วนระหว่าจำนวนนิวตรอนต่อโปรตอนไม่เหมาะสม คือนิวเคลียสที่มีจำนวนนิวตรอนมาก หรือ น้อยกว่าจำนวนโปรตอนมักจะไม่เสถียรจะมีการแผ่รังสีออกมาจนได้ไอโชโทปของธาตุใหม่ที่เสถียรกว่า นอกจากนั้นยังพบว่าจำนวนโปรตอนและนิวตรอนที่เป็นจำนวนคู่ หรือคี่ในนิวเคลียสนั้น มีความสัมพันธ์กับความเสถียรภาพของนิวเคลียสด้วย กล่าวคือ ไอโชโทปของธาตุที่มีจำนวนโปรตอน และนิวตรอนเป็นเลขคู่ จะเสถียรกว่าไอโชโทปของธาตุที่มีจำนวนโปรตอนและนิวตอนเป็นเลขคี่เช่น 714N เป็นไอโซโทปที่เสถียร 715N พบว่า 714N มีจำนวนโปรตอนและจำนวนนิวตรอน จึงเสถียรกว่า 715Nที่มีจำนวนโปรตอนไม่เท่ากับจำนวนนิวตรอน816O เป็นไอโซโทปที่เสถียรกว่า817O เพราะ 816O มีจำนวนโปรตอนและจำนวนนิวตรอนเท่ากัน จึงเสถียรกว่า817O ที่มีจำนวนนิวตรอนเป็นเลขคี่ และจำนวนโปรตอนเป็นเลขคู่
ธาตุกัมมันตรังสีในธรรมชาติ
ธาตุต่างๆที่พบในธรรมชาตินั้น ธาตุที่มีเลขอะตอมตั้งแต่ 83 ขึ้นไป ส่วนใหญ่สามารถแบ่งรังสีได้เช่น92238U 92235U 90232Th 86222Rn หรืออาจจะเขียนเป็น U-238, U-235, Th-232, Rn-222
นอกจากธาตุกัมมันตรังสีจะพบในธรรมชาติแล้ว นักวิทยาศาสตร์ยังสังเคราะห์ธาตุกัมมันตรังสีขึ้น
เพื่อใช้ประโยชน์ในด้านต่างๆอีกด้วย ซึ่งมีหลายวิธี แต่มีวิธีหนึ่งคือยิงนิวเคลียสของไอโซโทปที่เสถียรด้วยอนุภาคที่เหมาะสม และมีความเร็วสูง ได้ไอโซโทปของธาตุใหม่ที่เสถียร เช่น รัทเทอร์ฟอร์ด ได้ยิงนิวเคลียส N-14 ด้วยอนุภาคแอลฟา เกิด O-17
เขียนแผนภาพแทน คือ 14N( ) 17O ไอโซโทป817O ที่เสถียร พบในธรรมชาติ0.037%
การแผ่รังสีแอลฟา
เมื่อไอโซโทปกัมมันตรังสีให้อนุภาคแอลฟา นิวเคลียสของไอโซโทปเสีย 2 โปรตอน และ 2
นิวตรอน ดังนั้น ไอโซโทปกัมมันตรังสีจะเปลี่ยนไปเป็นธาตุอื่นที่มีเลขเชิงอะตอมต่ำกว่าเดิม 2 อะตอมและมีมวลต่ำกว่าเดิม 4 amu ตัวอย่างเช่น เมื่อ 92238U ให้อนุภาคแอลฟา ผลที่เกิดขึ้นจะให้ 90234Th สมการของปฏิกิริยาที่เกิดขึ้นเป็นดังนี้
92238U 24He+90234Th
จากสมการจะเห็นว่า ผลรวมของเลขเชิงอะตอมของด้านหนึ่งของสมการจะเท่ากันกับผลรวมของเลขเชิงอะตอมของอีกด้านหนึ่งของสมการ หรือ 92=2+90 ส่วนผลรวมของเลขมวลจะเท่ากันทั้ง 2 ด้านของสมการเช่นเดียวกันหรือ 238=4+234
การแผ่รังสีบีตา
การให้รังสีบีตาจะเกิดนิวเคลียสที่มีสัดส่วนของจำนวนนิวตรอนมากกว่าโปรตอน ตัวอย่างเช่น การแผ่รังสีบีตาของC-14 ไปเป็น N-14 C-14 ให้อนุภาคบีตา อนุภาคบีตาหรืออิเล็กตรอนเชื่อกันว่ามาจากนิวเคลียส เมื่อนิวตรอนสลายตัวไปเป็นโปรตอน 11H และอิเล็กตรอนดังนี้
01n----------> 11H+-10e
เมื่อ อิเล็กตรอนเกิดขึ้น อิเล็กตรอนจะถูกปล่อยออกจากนิวเคลียสด้วยความเร็วสูงแต่โปรตอนยังคงอยู่ผล ที่เกิดขึ้นทำให้นิวเคลียสมีจำนวนนิวตรอนลดลงไป 1 นิวตรอน และมีโปรตอนเพิ่มขึ้นอีก 1 โปรตอน ในกรณี C-14 ให้อนุภาคบีตา สมการ นิวเคลียร์จะเป็นดังนี้
614C------- >714 N+-10e
จากสมการจะเห็นว่าเลขเชิงอะตอมเพิ่มขึ้น 1 หน่วย และเลขมวลมีค่าคงที่
การแผ่รังสีแกมมา
การ ให้อนุภาคแอลฟาหรืออนุภาคอย่างใดอย่างหนึ่ง มักจะติดตามด้วยการแผ่รังสีแกมมา รังสีแกมมาถูกปล่อยออกมาเมื่อนิวเคลียสเปลี่ยนจากสถานะเร้าหรือสถานะพลังงาน สูง ไปยังสถานะที่มีพลังงานต่ำกว่าเนื่องจากรังสีแกมมาไม่มีทั้งประจุและมวล การแผ่รังสีแกมมาจึงไม่ทำให้มีการเปลี่ยนแปลงเลขมวลหรือเลขเชิงอะตอมของ นิวเคลียสอย่างใดอย่างหนึ่ง รังสีแกมมานำไปใช่รักษาโรค เป็นรังสีแกมมาที่มาจากเทคนิเทียม
4399Tc------> 4399Tc+y
เมื่อ Ra-226เปลี่ยนไปเป็น Rn-222 โดยการแผ่รังสีแอลฟานั้น Rn-222 ไม่เสถียรภาพจึงแผ่รังสีแกมมาออกมา
ครึ่งชีวิตของธาตุกัมมันตรังสี
ครึ่งชีวิตของธาตุ (half life) หมายถึง ระยะเวลาที่สารสลายตัวไปจนเหลือเพียงครึ่งหนึ่งของปริมาณเดิมใช้สัญลักษณ์เป็น t1/2 นิวเคลียสของธาตุกัมมันตรังสีที่ไม่เสถียร จะสลายตัวและแผ่รังสีได้เองตลอดเวลาโดยไม่ขึ้นอยู่กับอุณหภูมิหรือความดัน อัตราการสลายตัว เป็นสัดส่วนโดยตรงกับจำนวนอนุภาคในธาตุกัมมันตรังสีนั้น ปริมาณการสลายตัวจะบอกเป็นครึ่งชีวิตเป็นสมบัติเฉพาะตัวของแต่ละไอโซโทป
ตัวอย่างเช่น C-14 มีครึ่งชีวิต 5730 ปี หมายความว่า ถ้ามี C-14 1 กรัม เมื่อเวลาผ่านไป 5730 ปี จะเหลือ C-14 อยู่ 0.5 กรัม และเมื่อเวลาผ่านไปอีก 5730 ปี จะเหลืออยู่ 0.25 กรัม เป็นดังนี้ไปเรื่อยๆ กล่าวได้ว่าทุกๆ 5730 ปี จะเหลือ C-14 เพียงครึ่งหนึ่งของปริมาณเดิมครึ่งชีวิตเป็นสมบัติเฉพาะตัวของแต่ละไอโซโทป และสามารถใช้เปรียบเทียบอัตราการสลายตัวของธาตุกัมมันตรังสีแต่ละชนิดได้ ตัวย่างครึ่งชีวิตของไอโซโทปกัมมันตรังสีบางชนิด ครึ่งชีวิตของธาตุกัมมันตรังสีชนิดต่างๆมีค่าไม่เท่ากัน เช่น เทคนีเทียม -99 มีครึ่งชีวิต 6 ชั่วโมงเท่านั้น ส่วนยูเรเนียม -235 มีครึ่งชีวิต 4.5 ล้านปี
ครึ่งชีวิต (half life) ของสารกัมมันตรังสี สามารถนำไปใช้หาอายุอายุสัมบูรณ์ (Absolute Age) เป็นอายุของหินหรือซากดึกดำบรรพ์ ที่สามารถบอกจำนวนปีที่ค่อนข้างแน่นอน การหาอายุสัมบูรณ์ใช้วิธีคำนวณจากครึ่งชีวิต ของธาตุกัมมันตรังสีที่มีอยู่ในหิน หรือซากดึกดำบรรพ์ที่ต้องการศึกษา ธาตุกัมมันตรังสีที่นิยมนำมาหาอายุสัมบูรณ์ได้แก่ ธาตุคาร์บอน – 14 ธาตุโพแทศเซียม – 40 ธตาเรเดียม – 226 และธาตุยูเรเนียม – 238 เป็นต้น การหาอายุสัมบูรณ์มักใช้กับหินที่มีอายุมากเป็นแสนล้านปี เช่น หินแกรนิตบริเวณฝั่งตะวันตกของเกาะภูเก็ต ซึ่งเคยเป็นหินต้นกำเนิดแร่ดีบุกมีอายุสัมบูรณ์ประมาณ 100 ล้านปี ส่วนตะกอนและซากดึกดำบรรพ์ที่มีอายุน้อยกว่า 50,000 ปี มักจะใช้วิธีกัมมันตภาพรังสีคาร์บอน – 14 เช่น ซากหอยนางรมที่วัดเจดีย์หอย อำเภอลาดหลุมแก้ว จังหวัดปทุมธานี มีอายุประมาณ 5,500 ปีของวัตถุโบราณ
นอกจากนั้นยังใช้คำนวณอายุของโลก พบว่าว่าประมาณครึ่งหนึ่งของยูเรเนียมที่มีมาแต่แรกเริ่มได้สลายตัวเป็นตะกั่วไปแล้ว ดังนั้นอายุของโลกคือประมาณครึ่งชีวิตของยูเรเนียม หรือราว 4,500 ล้านปี
ประโยชน์ของครึ่งชีวิต
ครึ่งชีวิตสามารถใช้หาอายุของวัตถุโบราณที่มีธาตุคาร์บอนเป็นองค์ประกอบ เรียกว่าวิธี Radiocarbon Dating ซึ่งคำว่า dating หมายถึง การหาอายุจึงมักใช้หาอายุของวัตถุโบราณที่มีคุณค่าทางประวิติศาสตร์
หลักการสำคัญของการหาอายุวัตถุโบราณโดยวิธี Radiocarbon Dating เป็นหลักการที่อาศัยความรู้เกี่ยวกับกัมมันตภาพรังสีที่เกิดขึ้นเองในอากาศ ตัวการที่สำคัญคือ รังสีคอสมิก ซึงอยู่ในบรรยากาศเหนือพื้นโลก มีความเข้มสูงจนทำให้นิวเคลียสขององค์ประกอบของอากาศแตกตัวออก ให้อนุภาคนิวตรอน แล้วอนุภาคนิวตรอนชนกับไนโตรเจนในอากาศ
ข้อควรจำ
1. ในทางปฏิบัติการวัดหาจำนวนนิวเคลียสโดยตรงกระทำได้ยาก และเนื่องจากจำนวนนิวเคลียสในสารหนึ่ง ๆ จะเป็นสัดส่วนกับปริมาณของสารนั้น ๆ ดังนั้นจึงพิจารณาเป็นค่ากัมมันตภาพหรืการวัดมวลแทน ดังนี้
โดยที่ A0 คือกัมมันตภาพที่เวลาเริ่มต้น (t=0)
โดยที่ m0 คือมวลสารตั้งต้นที่เวลาเริ่มต้น (t=0)
ประโยชน์และโทษของธาตุกัมมันตรังสี
ในทางอุตสาหกรรม ใช้รังสีวัดวามหนาของวัสดุในโรงงานผลิตกระดาษ ผลิตแผ่นยาง และแผ่นโลหะ ใช้รังสีในการวิเคราะห์ส่วนประกอบของผลิตภัณฑ์ เช่น โลหะผสม แร่ ถ่านหิน และตรวจสอบรอยเชื่อม–รอนร้าวในโลหะหรือโครงสร้างอาคาร ใช้ยูเรเนียมเป็นเชื้อเพลิงสำหรับผลิตกระแสไฟฟ้าในโรงไฟฟ้านิวเคลียร์
ทางการเกษตร ใช้รังสีในการถนอมอาหารเพื่อยืดอายุการเก็บรักษาอาหาร เพราะรังสีจะทำลายแบคทีเรียและจุลินทรีย์ที่ก่อให้เกิดการเน่าเสียในอาหาร ใช้รังสีเพื่อปรับปรุงพันธุ์พืชให้มีความแข็งแรงต้านทานต่อโรคและแมลง เพื่อเพิ่มผลผลิตให้สูงขึ้น
จะเห็นได้ว่าธาตุกัมมันตรังสีให้ประโยชน์ต่อมนุษย์อย่างมาก แต่ถ้าใช้ไม่เหมาะสม เช่น ทำระเบิดนิวเคลียร์ก็จะเป็นมหันตภัยร้ายแรง ดังนั้น การใช้ธาตุกัมมันตรังสีจึงมีทั้งประโยชน์และโทษ
การเกิดกัมมันตรังสี
ธาตุอีกกลุ่มหนึ่งในตารางธาตุซึ่งมีสมบัติแตกต่างจากธาตุที่เคยศึกษามาแล้ว กล่าวคือสามารถแผ่รังสีแล้วกลายเป็นอะตอมของธาตุใหม่ได้ การเปลี่ยนแปลงเหล่านี้เกิดขึ้นได้อย่างไร
ในปี ค.ศ. 1896 (พ.ศ.2439) อองตวน อองรีแบ็กเกอเรล นักวิทยาศาสตร์ชาวฝรั่งเศส พบว่าเมื่อเก็บแผ่นฟิล์มถ่ายรูปที่หุ้มด้วยกระดาษสีดำไว้กับสารประกอบของยูเรเนียม ฟิล์มจะมีลักษณะเหมือนถูกแสง และเมื่อทำการทดลองมีสารประกอบของยูเรเนียมชนิดอื่นๆ ก็ได้ผล เช่นเดียวกัน จึงสรุปว่าน่าจะมีรังสีแผ่ออกมาจากธาตุยูเรเนียม
ต่อมาปีแอร์ และมารี กูรี ได้ค้นพบว่าธาตุพอโลเนียมเรเดียม และทอเรียม ก็สามารถแผ่รังสีได้เช่นเดียวกันปรากฎการณ์ที่ธาตุแผ่รังสีได้เองอย่างต่อเนื่องเช่นนี้เรียกว่า กัมมันตภาพรังสี เป็นการเปลี่ยนแปลงภายในนิวเคลียสของไอโซโทปที่ไม่เสถียร และเรียกธาตุที่มีสมบัติเช่นนี้ว่า ธาตุกัมมันตรังสี ธาตุกัมมันตรังสีส่วนใหญ่มีเลขอะตอมสูงกว่า 83 แต่มีธาตุกัมมันตรังสีบางชนิดที่มีเลขอะตอมน้อยกว่า 83 เช่น 43pt ในธรรมชาติพบธาตุกัมมันตรังสีหลายชนิดเช่น 238๊U 235๊U 232 Th และ 222Rn หรืออาจเขียน U-238 U-235 Th-232 และ Rn-222 ก็ได้ นอกจากนี้นักวิทยาศาสตร์ยังสังเคราะห์ธาตุกัมมันตรังสีขึ้นเพื่อใช้ประโยชน์ในด้านต่างๆ ได้อีก
1. การเกิดกัมมันตภาพรังสี
กัมมันตภาพรังสีเป็นปรากฎการณ์ทางธรรมชาติของสาร เกิดจากธาตุกัมมันตรังสี เช่น U-238 และ Th-232 แผ่รังสีออกมาตลอดเวลา ทั้งนี้เพราะนิวเคลียสของธาตุกัมมันตรังสีมีพลังงานสูงมากและไม่เสถียร จึงปล่อยพลังงานออกมาในรูปของอนุภาคหรือรังสีบางชนิด แล้วธาตุเหล่านั้นก็จะเปลี่ยนเป็นธาตุใหม่ ต่อมารัทเทอร์ฟอร์ดได้ศึกษาเพิ่มเติมและแสดงให้เห็นว่ารังสีที่แผ่ออกมาจากธาตุกัมมันตรังสีอาจเป็นรังสีแอลฟา บีตาหรือแกมมา ที่มีสมบัติแตกต่างกันดังตาราง 3.1
ตาราง 3.1 ชนิดและสมบัติของรังสีบางชนิด

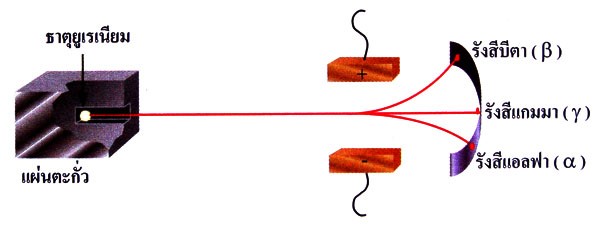
รูป 1.1 ผลของสนามไฟฟ้าต่อรังสีทั้ง 3 ชนิด
นอกจากนี้ยังมีรังสีชนิดอื่นๆ เช่น โพซิตรอน สัญลักษณ์คือโปรตอน(p) สัญลักษณ์คือดิวเทอรอน (D) สัญลักษณ์คือทริทอน (T) สัญลักษณ์คือและนิวตรอน (n) สัญลักษณ์คือ
2. การสลายตัวของธาตุกัมมันตรังสี
จากการศึกษาไอโซโทปของธาตุจำนวนมากทำให้ได้ข้อสังเกตว่า ไอโซโทปของนิวเคลียสที่มีอัตราส่วนระหว่างจำนวนนิวตรอนต่อจำนวนโปรตอนไม่เหมาะสมคือนิวเคลียสที่มีจำนวนนิวตรอนแตกต่างจากจำนวนโปรตอนมากเกินไปจะไม่เสถียร จึงเกิดการเปลี่ยนแปลงภายในนิวเคลียสแล้วเกิดเป็นนิวเคลียสของธาตุใหม่ที่เสถียรกว่าโดยการแผ่รังสีออกมา ดังตัวอย่างต่อไปนี้
การแผ่รังสีแอลฟา ส่วนใหญ่เกิดกับนิวเคลียสที่มีและอะตอมสูงกว่า 82 และมีจำนวนนิวตรอนต่อโปรตอนในสัดส่วนที่ไม่เหมาะสม เมื่อปล่อยรังสีแอลฟาออกมาจะกลายเป็นนิวเคลียสของธาตุใหม่ที่เสถียรซึ่งมีเลขอะตอมลดลง 2 เลขมวลลดลง 4 ดังตัวอย่าง
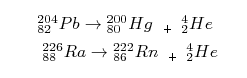
การแผ่รังสีบีตา เกิดกับนิวเคลียสที่มีจำนวนนิวตรอนมากกว่าโปรตอน นิวตรอนในนิวเคลียสจะเปลี่ยนไปเป็นโปรตอนและอิเล็กตรอน เมื่อปล่อยรังสีบีตาออกมานิวเคลียสใหม่จะมีเลขอะตอมเพิ่มขึ้น 1 เลขมวลยังคงเดิมดังตัวอย่าง
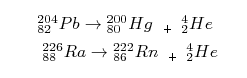
การแผ่รังสีแกมมา เกิดกับไอโซโทปกัมมันตรังสีที่มีพลังงานสูงมาก หรือไอโซโทปที่สลายตัวให้รังสีแอลฟาหรือบีตา แต่นิวเคลียสที่เกิดใหม่ยังไม่เสถียรเพราะมีพลังงานสูงจึงเกิดการเปลี่ยนแปลงในนิวเคลียสเพื่อให้มีพลังงานต่ำลงโดยปล่อยพลังงานส่วนเกินออกมาเป็นรังสีแกมมาดังตัวอย่าง
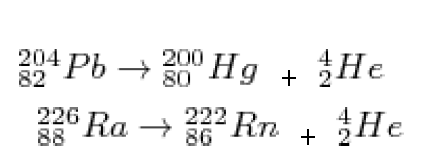
นิวเคลียสของไอโซโทปกัมมันตรังสีสามารถสลายตัวและแผ่รังสีได้ตลอดเวลาโดยไม่ขึ้นกับอุณหภูมิหรือความดัน การสลายตัวและแผ่รังสีของไอโซโทปกัมมันตรังสีจะเป็นสัดส่วนโดยตรงกับจำนวนอนุภาคในนิวเคลียสกัมมันตรังสีนั้น นักเรียนคิดว่าธาตุกัมมันตรังสีต่างชนิดกันจะมีอัตราการสลายตัวแตกต่างกันหรือไม่ วัดปริมาณการสลายตัวได้อย่างไร
3. ครึ่งชีวิตของธาตุกัมมันตรังสี
ธาตุกัมมันตรังสีจะสลายตัวให้รังสีชนิดใดชนิดหนึ่งออมาได้เองตลอดเวลา ธาตุกัมมันตรังสีแต่ละชนิดจะสลายตัวได้เร็วหรือช้าแตกต่างกัน ปริมาณการสลายตัวของธาตุกัมมันตรังสีจะบอกเป็น ครึ่งชีวิต ใช้สัญลักษณ์ครึ่งชีวิต หมายถึง ระยะเวลาที่นิวเคลียสของธาตุกัมมันตรังสี สลายตัวจนเหลือครึ่งหนึ่งของปริมาณเดิม ไอโซโทปกัมมันตรังสีของธาตุชนิดหนึ่งๆ จะมีครึ่งชีวิตคงเดิมไม่ว่าจะอยู่ในรูปของธาตุหรือเกิดเป็นสารประกอบ เช่น Na-24 มีครึ่งชีวิต 15 ชั่วโมง หมายความว่าถ้าเริ่มต้นมี Na-24 10 กรัม นิวเคลียสนี้จะสลายตัวให้รังสีออกมาจนกระทั่งเวลาผ่านไปครบ 15 ชั่วโมง จะมี Na-24 เหลือ 5 กรัม และเมื่อเวลาผ่านไปอีก 15 ชั่วโมงจะมี Na-24 เหลืออยู่ 2.5 กรัม นั้นคือเวลาผ่านไปทุกๆ 15 ชั่วโมง Na-24 จะสลายตัวไปเหลือเพียงครึ่งหนึ่งของปริมาณเดิมเขียนแสดงได้ดังรูป 3.6
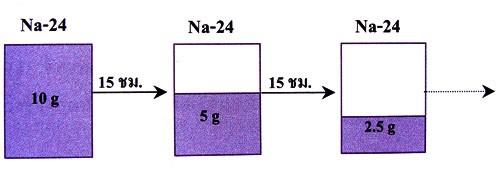
รูป 1.2 แสดงปริมาณของ Na-24 ที่ลดลงครึ่งหนึ่งทุกๆ 15 ชั่วโมง
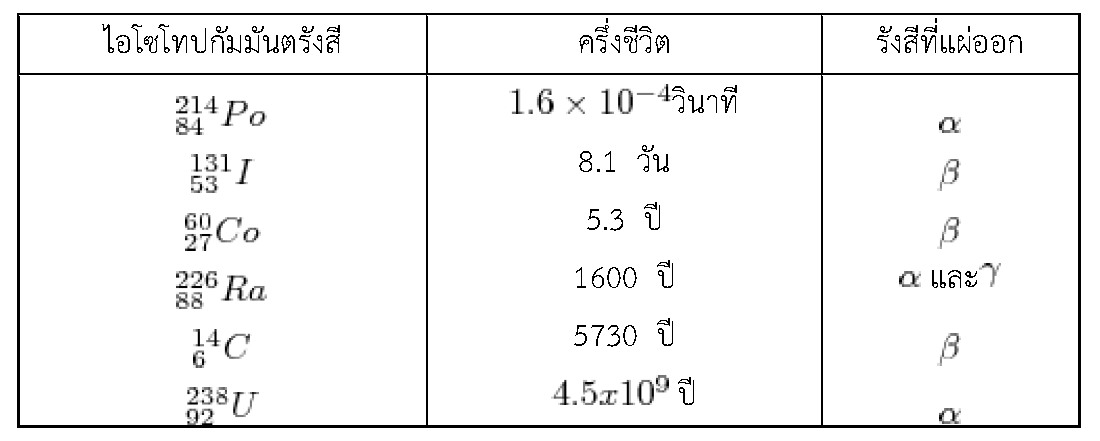
ครึ่งชีวิตเป็นสมบัติเฉพาะตัวของแต่ละไอโซโทปและสามารถใช้เปรียบเทียบอัตราการสลายตัวของธาตุกัมมันตรังสีแต่ละชนิดได้ ตัวอย่างครึ่งชีวิตของไอโซโทปกัมมันตรังสีบางชนิด แสดงดังตาราง 3.12
ตาราง 3.2 ตัวอย่างครึ่งชีวิตของไอโซโทปกัมมันตรังสีบางชนิด


ไม่มีความคิดเห็น:
แสดงความคิดเห็น